2.下列有关化学用语使用正确的是( )
| A. | CO2的球棍模型: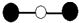 | B. | 乙烷的结构式CH3-CH3 | ||
| C. | 新戊烷的结构简式:C(CH3)4 | D. | CCl4的电子式: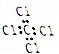 |
20.下列有关电解质溶液的说法中错误的是( )
| A. | 0.1mol•L-1的HCl溶液的pH=1 | |
| B. | 0.1mol•L-1的CH3COOH溶液中c(H+)<0.1mol•L-1 | |
| C. | 0.1mol•L-1的CH3COOH溶液和0.1mol•L-1的NaOH溶液等体积混合后溶液的pH=7 | |
| D. | 100mL0.1mol•L-1的H2SO4溶液中慢慢滴入100mL0.1mol•L-1的Ba(OH)溶液后,混合溶液的导电性几乎为零 |
19.0.5LFeCl3溶液中Cl-为9.03×1023个,则FeCl3溶液的物质的量浓度为( )
| A. | 0.1mol•L-1 | B. | 1mol•L-1 | C. | 3mol•L-1 | D. | 1.5mol•L-1 |
16.磷酸盐缓冲溶液对维持生物体内的正常pH和正常生理环境起重要作用.将0.2mol•L-1的NaH2PO4与0.2mol•L-1的Na2HPO4溶液以不同比例混合,可形成不同pH的缓冲溶液.
试回答下列问题:
(1)在pH=5.9的磷酸盐缓冲溶液中,c(Na+)=0.22mol/L(溶液混合时的体积变化忽略不计).
(2)欲直接利用NaH2PO4•2H2O和Na2HPO4•2H2O配制100mLpH=5.8的NaH2PO4-Na2HPO4缓冲溶液,需称量NaH2PO4•2H2O、Na2HPO4•2H2O的质量分别为2.87g、0.285g.
| pH | NaH2PO4溶液体积/mL | Na2HPO4溶液体积/mL |
| 5.7 | 93.5 | 6.5 |
| 5.8 | 92 | 8 |
| 5.9 | 90 | 10 |
| 6.0 | 87.7 | 12.3 |
(1)在pH=5.9的磷酸盐缓冲溶液中,c(Na+)=0.22mol/L(溶液混合时的体积变化忽略不计).
(2)欲直接利用NaH2PO4•2H2O和Na2HPO4•2H2O配制100mLpH=5.8的NaH2PO4-Na2HPO4缓冲溶液,需称量NaH2PO4•2H2O、Na2HPO4•2H2O的质量分别为2.87g、0.285g.
14.少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,以下方法中可行的是( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴加几滴硫酸铜溶液
⑦从常温升高到30℃(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L的盐酸.
0 157616 157624 157630 157634 157640 157642 157646 157652 157654 157660 157666 157670 157672 157676 157682 157684 157690 157694 157696 157700 157702 157706 157708 157710 157711 157712 157714 157715 157716 157718 157720 157724 157726 157730 157732 157736 157742 157744 157750 157754 157756 157760 157766 157772 157774 157780 157784 157786 157792 157796 157802 157810 203614
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴加几滴硫酸铜溶液
⑦从常温升高到30℃(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L的盐酸.
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ⑤⑥⑧ |