1.某同学完成如下探究实验:
实验目的:比较Cl2、Br2、I2三种单质的氧化性强弱
实验药品:NaBr溶液、KI溶液、氯水、淀粉溶液
实验记录:
反思与评价:
(1)步骤①反应的离子方程式为:2Br-+Cl2=Br2+2Cl-.
(2)检验②中所得黄色溶液含I2的另一种方法是(简述实验操作和相应的实验现象)
向溶液中加入CCl4,振荡,静置,液体分为上下两层,下层呈紫红色.
(3)你认为上述实验设计(填“能”或“不能”)不能达到实验目的,理由是①中所得黄色溶液中可能含有Cl2,会干扰Br2、I2氧化性的比较.
实验目的:比较Cl2、Br2、I2三种单质的氧化性强弱
实验药品:NaBr溶液、KI溶液、氯水、淀粉溶液
实验记录:
| 实验步骤 | 实验现象 | 实验结论 |
 | 溶液变为黄色 | 氧化性:Cl2>Br2 |
 | 溶液变为黄色 | 氧化性: Br2>I2 |
 | 溶液的颜色由黄色变为蓝色 |
(1)步骤①反应的离子方程式为:2Br-+Cl2=Br2+2Cl-.
(2)检验②中所得黄色溶液含I2的另一种方法是(简述实验操作和相应的实验现象)
向溶液中加入CCl4,振荡,静置,液体分为上下两层,下层呈紫红色.
(3)你认为上述实验设计(填“能”或“不能”)不能达到实验目的,理由是①中所得黄色溶液中可能含有Cl2,会干扰Br2、I2氧化性的比较.
15.NaCl是重要的化工原料,可以制备一系列物质.有关下列流程的说法中,正确的是( )

| A. | NaHCO3的热稳定性好 | |
| B. | 如图所示转化涉及的反应都是氧化还原反应 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
14.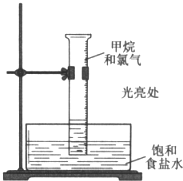 甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
 甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )| 现象 | 解释 | |
| A. | 量筒内气体颜色逐渐变浅 | 甲烷被氯气还原 |
| B. | 量筒内出现少量白雾 | 生成HCl气体 |
| C. | 量筒内壁产生油状液滴 | 油状液体是CCl4 |
| D. | 量筒中液面降低 | 生成液态产物 |
| A. | A | B. | B | C. | C | D. | D |
13.下列实验操作和现象与结论关系不正确的是( )
0 157610 157618 157624 157628 157634 157636 157640 157646 157648 157654 157660 157664 157666 157670 157676 157678 157684 157688 157690 157694 157696 157700 157702 157704 157705 157706 157708 157709 157710 157712 157714 157718 157720 157724 157726 157730 157736 157738 157744 157748 157750 157754 157760 157766 157768 157774 157778 157780 157786 157790 157796 157804 203614
| 操作和现象 | 结论 | |
| A. | 将大小相同的K和Na放入等体积的水中,钾比钠反应剧烈 | 钾元素的金属性比钠元素强 |
| B. | 将Ba(OH)2•8H2O和NH4Cl晶体在小烧杯中混合搅拌,用手触摸烧杯外壁感觉变凉 | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 |
| C. | 在催化剂存在的条件下,石蜡油加强热生成的气体通入溴的四氯化碳溶液中,溶液褪色 | 石蜡油的分解产物都是烯烃 |
| D. | 向盛有H2O2溶液的试管中,加入少量FeCl3溶液,产生气泡的速率比不加FeCl3溶液的快 | FeCl3可以加快H2O2分解的速率,起了催化作用 |
| A. | A | B. | B | C. | C | D. | D |

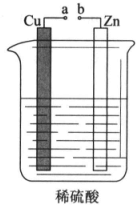 课外小组的同学对如图所示的实验装置进行了研究.
课外小组的同学对如图所示的实验装置进行了研究.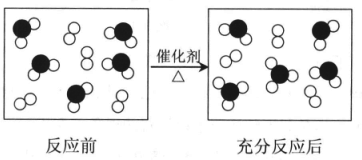
 ,该化合物中含有极性共价键(填“极性”或“非极性”).
,该化合物中含有极性共价键(填“极性”或“非极性”).