15.下列实验能获得成功的是( )
| A. | 苯与浓溴水反应制溴苯 | |
| B. | 向苯酚稀溶液中加过量饱和溴水观察沉淀 | |
| C. | 将乙醛滴入银氨溶液中,直接加热煮沸制银镜 | |
| D. | 1mol•L-1的CuSO4溶液2mL和0.5mol•L-1的NaOH溶液4mL混合后,加入40%的乙醛溶液0.5mL,加热煮沸观察沉淀颜色 |
14.如图反应能说明酚分子中由于羟基影响苯环,使苯酚分子中苯环比苯活泼的是( )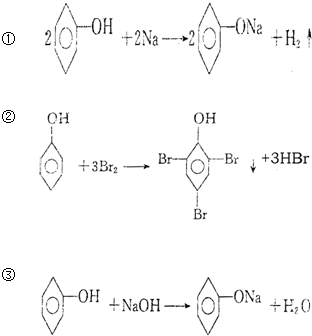

| A. | ①③ | B. | 只有② | C. | ②和③ | D. | 全部 |
13.乙醇分子结构中,各化学键如图所示.关于乙醇在各种反应中断键的说法不正确的是( )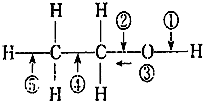

| A. | 和金属钠反应时断裂① | |
| B. | 乙醇燃烧时断裂②和⑤ | |
| C. | 在银催化条件下,与O2反应时断裂①和③ | |
| D. | 和浓H2SO4、乙酸共热时断裂①,其他键不变化 |
12.某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极是否相同?否(用“是”或“否”回答);
(2)写出实验3中的电极名称和电极反应式:
铝为负极极,2Al-6e-═2Al3+;
石墨为正极,6H++6e-═3H2↑(;
(3)实验4中的铝为负极,写出电池总反应方程式2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(4)解释实验5中灵敏电流计指针偏向铝的原因:Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电子由负极流向正极,所以电流计指针偏向铝
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?自发的氧化还原反应中金属铝是否参与反应,金属铝参加反应,失电子,做负极,反之作正极,与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关.
| 编号 | 电极材料 | 电解质溶液 | 灵敏电流计指针偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极是否相同?否(用“是”或“否”回答);
(2)写出实验3中的电极名称和电极反应式:
铝为负极极,2Al-6e-═2Al3+;
石墨为正极,6H++6e-═3H2↑(;
(3)实验4中的铝为负极,写出电池总反应方程式2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(4)解释实验5中灵敏电流计指针偏向铝的原因:Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电子由负极流向正极,所以电流计指针偏向铝
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?自发的氧化还原反应中金属铝是否参与反应,金属铝参加反应,失电子,做负极,反之作正极,与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关.
11.A、B、C、D、E是五种短周期元素.已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等.甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子.
请回答下列问题:
(1)C的最低价氢化物与乙相比较,稳定性强弱关系(用相应的化学式表示):H2O>CH4
(2)元素E在周期表中的位置为第三周期VIIA族
(3)请写出两种与乙具有相同电子数的非单核离子的化学式:NH4+和OH-
(4)把D的单质放到NaOH溶液中,反应的化学方程式为:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(5)写出甲的电子式: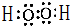
(6)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)=0.2mol•L-1,c(Cl-)=1.3mol•L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4mol•L-1 NaOH 溶液的体积是:80mL.
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 各元素原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
(1)C的最低价氢化物与乙相比较,稳定性强弱关系(用相应的化学式表示):H2O>CH4
(2)元素E在周期表中的位置为第三周期VIIA族
(3)请写出两种与乙具有相同电子数的非单核离子的化学式:NH4+和OH-
(4)把D的单质放到NaOH溶液中,反应的化学方程式为:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(5)写出甲的电子式:
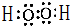
(6)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)=0.2mol•L-1,c(Cl-)=1.3mol•L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4mol•L-1 NaOH 溶液的体积是:80mL.
10.下列关于化学键说法正确的是( )
| A. | 构成单质分子的微粒中不一定含有化学键 | |
| B. | 只含有共价键的物质一定是共价化合物 | |
| C. | NaCl溶于水破坏了离子键,乙醇溶于水破坏了共价键 | |
| D. | CaCl2中既有共价键又有离子键 |
9.某温度时,浓度都是1mol/L的两种气体X2、Y2在密闭容器中反应生成气体Z达平衡后,c (X2)为0.4mol/L,c (Y2)为0.8mol/L,生成c (Z)为0.4mol/L,则该反应的反应式(z用x、y表示)是( )
| A. | X2+2Y2 ?2XY2 | B. | 2X2+Y2 ?2X2Y | C. | 3X2+Y2?2X3Y | D. | X2+3Y2?2XY3 |
8.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
0 157592 157600 157606 157610 157616 157618 157622 157628 157630 157636 157642 157646 157648 157652 157658 157660 157666 157670 157672 157676 157678 157682 157684 157686 157687 157688 157690 157691 157692 157694 157696 157700 157702 157706 157708 157712 157718 157720 157726 157730 157732 157736 157742 157748 157750 157756 157760 157762 157768 157772 157778 157786 203614
| A. | CO2的电子式: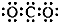 | |
| B. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| C. | NH4Cl的电子式: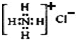 | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
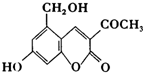 “亮菌甲素”的结构简式为如图所示,它配以辅料丙二1,3,5醇溶成针剂用于临床,而假药“亮菌甲素”是用廉价的二甘醇作为辅料.二甘醇为工业溶剂,有很强的毒性,会使肾功能衰竭.请回答下列问题:
“亮菌甲素”的结构简式为如图所示,它配以辅料丙二1,3,5醇溶成针剂用于临床,而假药“亮菌甲素”是用廉价的二甘醇作为辅料.二甘醇为工业溶剂,有很强的毒性,会使肾功能衰竭.请回答下列问题: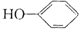 合成
合成 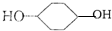
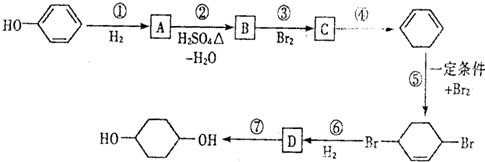
 ,D
,D .
.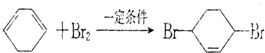 写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学反应方程式
写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学反应方程式 .
.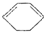 的反应方程式(有机物写结构简式,注明反应条件).
的反应方程式(有机物写结构简式,注明反应条件). .
.