15. 某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
(1)称取13.0 g草酸晶体,配成250 mL水溶液.此操作过程必须用到的2种定量仪器是托盘天平和250mL容量瓶.
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①配平离子方程式:MnO${\;}_{4}^{-}$+H2C2O4+H+→Mn2++CO2↑+H2O
②滴定达到终点的标志是加入最后一滴高锰酸钾溶液,锥形瓶内溶液由无色变为红色,且半分钟不褪色.
(3)按正确操作测得有关数据记录如下:
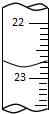
①a的读数如图所示,则a=22.80;
②草酸晶体的纯度为98.86%(结果保留两位小数).
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏低的是C.
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后未用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
 某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:(1)称取13.0 g草酸晶体,配成250 mL水溶液.此操作过程必须用到的2种定量仪器是托盘天平和250mL容量瓶.
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①配平离子方程式:MnO${\;}_{4}^{-}$+H2C2O4+H+→Mn2++CO2↑+H2O
②滴定达到终点的标志是加入最后一滴高锰酸钾溶液,锥形瓶内溶液由无色变为红色,且半分钟不褪色.
(3)按正确操作测得有关数据记录如下:
| 滴定次数 | 草酸溶液体积 | 酸性KMnO4溶液体积 | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.20 | 20.58 |
| 第二次 | 25.00 | 4.00 | 24.40 |
| 第三次 | 25.00 | 2.38 | a |
②草酸晶体的纯度为98.86%(结果保留两位小数).
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏低的是C.
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后未用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
14.在蒸发皿中加热蒸干并灼烧下列物质的溶液,可以得到该固体物质的是( )
| A. | KHCO3 | B. | AlCl3 | C. | Na2SO3 | D. | Fe2(SO4)3 |
13.下列有关实验的说法正确的是( )
| A. | 用pH试纸测得氯水的pH=2;用带磨口玻璃塞的试剂瓶保存K2CO3溶液 | |
| B. | 用酸式滴定管或移液管量取20.00 mL酸性K2Cr2O7溶液 | |
| C. | 用托盘天平称取5.85 g NaNO3晶体;用10mL量筒量取6.8mL稀H2SO4 | |
| D. | 酸碱中和滴定时,滴定管和锥形瓶都需用标准液或待测液润洗 |
12.一定温度下,水存在电离平衡H2O(l)?H+(aq)+OH-(aq),下列叙述一定正确的是( )
| A. | 向水中加入KHSO4溶液,平衡逆向移动,Kw减小 | |
| B. | 将水加热,Kw增大,pH减小,但还是中性 | |
| C. | 向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低 | |
| D. | 向水中加入AlCl3溶液,平衡向右移动,KW增大 |
11.下列属于强电解质,且能导电的是( )
| A. | 饱和食盐水 | B. | KNO3固体 | C. | 熔融的NaOH | D. | HCOOH |
8.下列方程式的书写正确的是( )
0 157588 157596 157602 157606 157612 157614 157618 157624 157626 157632 157638 157642 157644 157648 157654 157656 157662 157666 157668 157672 157674 157678 157680 157682 157683 157684 157686 157687 157688 157690 157692 157696 157698 157702 157704 157708 157714 157716 157722 157726 157728 157732 157738 157744 157746 157752 157756 157758 157764 157768 157774 157782 203614
| A. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ | |
| B. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32-通电 | |
| C. | 工业上用电解法制备烧碱:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| D. | NaHCO3溶液中HCO3-水解方程式:HCO3-+H2O?CO32-+H3O+ |
 、
、
 (其中任意一种).
(其中任意一种).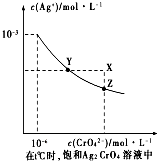 盐在化学工业中有重要的应用,请回答下列问题
盐在化学工业中有重要的应用,请回答下列问题 .
.