5. Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小.本实验中实验2和实验3表明温度对反应速率有影响,该因素对反应速率的具体影响是:其它条件相同时,温度越高反应速率越快.
(2)我们最好选取实验1、2和4(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的接触面积越大反应速率越快.
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是锌会置换出少量的金属铜,在该条件下构成了原电池,加快了反应速率.
(4)利用表中数据,可以求得:硫酸的物质的量浓度是2.0mol/L.
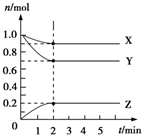
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.请通过计算回答下列问题:
(5)反应开始至2min,Y的平均反应速率0.03mol/(L•min).
(6)分析有关数据,写出X、Y、Z的反应方程式X(g)+3Y(g)?2Z(g).
 Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
(2)我们最好选取实验1、2和4(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的接触面积越大反应速率越快.
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是锌会置换出少量的金属铜,在该条件下构成了原电池,加快了反应速率.
(4)利用表中数据,可以求得:硫酸的物质的量浓度是2.0mol/L.
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.请通过计算回答下列问题:
(5)反应开始至2min,Y的平均反应速率0.03mol/(L•min).
(6)分析有关数据,写出X、Y、Z的反应方程式X(g)+3Y(g)?2Z(g).
4.下列有关化学反应速率的说法中,正确的是( )
| A. | 100 mL 2 mol/L盐酸与锌反应时,加入100 mL氯化钠溶液,生成氢气的速率不变 | |
| B. | 对于可逆反应2CO+2NO?N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 | |
| C. | 二氧化硫的催化氧化是一个放热反应,升高温度,正反应速率减慢 | |
| D. | 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快氢气的产生 |
3.下列说法一定不正确的是( )
| A. | 某些花岗石产生氡($\stackrel{222}{86}$Rn),从而对人体产生伤害,$\stackrel{222}{86}$Rn的质量数是222 | |
| B. | Se是人体必需的微量元素,$\stackrel{78}{34}$Se和$\stackrel{80}{34}$Se互为同位素 | |
| C. | $\stackrel{13}{6}$C-NMR(核磁共振)可用于含碳化合物的结构分析,$\stackrel{13}{6}$C的中子数为6 | |
| D. | 原子结构示意图 既可以表示16O,也可以表示18O 既可以表示16O,也可以表示18O |
2.已知:①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,与浓H2SO4能反应.可说明氯比硫的非金属性强的是( )
| A. | 全部 | B. | ②③④ | C. | ①②④ | D. | ②③④⑤ |
1.酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和 NH4Cl 等组成的糊状填充物.该电池放电过程产生 MnOOH.回收处理该废电池可得到多种化工原料.有关数据如表所示溶解度/(g/100g 水)
回答下列问题:
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+;.
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有 ZnCl2和NH4Cl,二者可通过加热浓缩、冷却结晶(填操作方法)分离回收;欲从滤渣中得到较纯的 MnO2,最简便的方法为在足量的空气或氧气中加热.
(3)用废电池的锌皮制备 ZnSO4•7H2O 的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀 H2SO4和 H2O2溶解,铁变为Fe3+,加碱调节至 pH 为3时,铁刚好沉淀完全(离子浓度小于 1×10-5 mol•L-1时,即可认为该离子沉淀完全);继续加碱至 pH 为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2后果是Zn2+和Fe2+不能分离.
0 157583 157591 157597 157601 157607 157609 157613 157619 157621 157627 157633 157637 157639 157643 157649 157651 157657 157661 157663 157667 157669 157673 157675 157677 157678 157679 157681 157682 157683 157685 157687 157691 157693 157697 157699 157703 157709 157711 157717 157721 157723 157727 157733 157739 157741 157747 157751 157753 157759 157763 157769 157777 203614
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+;.
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有 ZnCl2和NH4Cl,二者可通过加热浓缩、冷却结晶(填操作方法)分离回收;欲从滤渣中得到较纯的 MnO2,最简便的方法为在足量的空气或氧气中加热.
(3)用废电池的锌皮制备 ZnSO4•7H2O 的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀 H2SO4和 H2O2溶解,铁变为Fe3+,加碱调节至 pH 为3时,铁刚好沉淀完全(离子浓度小于 1×10-5 mol•L-1时,即可认为该离子沉淀完全);继续加碱至 pH 为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2后果是Zn2+和Fe2+不能分离.
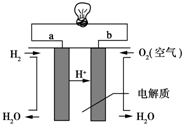 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.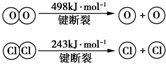 用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反应A中,4mol HCl被氧化,放出115.6kJ的热量.
用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反应A中,4mol HCl被氧化,放出115.6kJ的热量.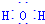 .
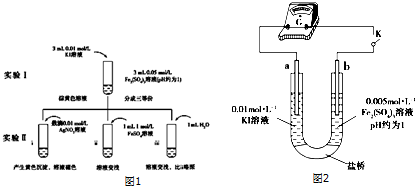
.
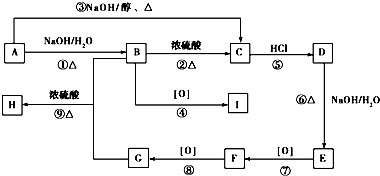
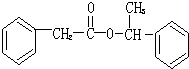 .
. .
. ,用化学方程式表示检验 F 中官能团的常用方法
,用化学方程式表示检验 F 中官能团的常用方法 .
.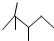 ,有机物 B 与等物质的量的 H2发生加成反应可得到有机物 A.则:
,有机物 B 与等物质的量的 H2发生加成反应可得到有机物 A.则: