17.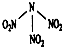 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )| A. | 分子中N、O间形成的共价键是非极性键 | |
| B. | 分子中四个氮原子共平面 | |
| C. | 该物质既有氧化性又有还原性 | |
| D. | 15.2g该物质含有6.02×1022个原子 |
16.下列物质的化学键类型、晶体类型与空间构型均相同的是( )
| A. | NaCl CsCl | B. | CO2 SiO2 | C. | BF3 SO3 | D. | CaF2BeCl2 |
15.下列说法错误的是( )
| A. | 离子化合物中可能存在单个小分子 | |
| B. | 两种非金属元素组成的晶体不可能是离子晶体 | |
| C. | 离子晶体中可能存在分子间作用力 | |
| D. | 离子晶体一定是离子化合物 |
14.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 体心立方是金属最密堆积形式 | |
| B. | NaCl晶体的配位数为4 | |
| C. | 24g金刚石中含有C-C键的个数为4NA | |
| D. | 中和热测定时,用铜棒代替环形玻璃棒会导致△H偏低 |
13.室温下,下列溶液的说法不正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
| pH | 11 | 11 | 3 | 3 |
| A. | 水的电离程度:①=②=③=④ | |
| B. | 分别加水稀释10倍,溶液的pH:①>②>③>④ | |
| C. | ①、③两溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | V1L②溶液与V2 L③溶液混合,若混合溶液pH=4,则V1:V2=9:11(忽略溶液体积变化) |
12.下列叙述中正确的是( )
| A. | pH=11的Na0H和Na2S溶液中水的电离程度前者大于后者 | |
| B. | 实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉 | |
| C. | 25℃,Cu(OH)2在水中的溶度积和溶解度比其在Cu(NO3)2溶液中的大 | |
| D. | 向FeCl3+3KSCN?Fe(SCN)3+3KCl平衡体系中加入少量KCl 固体,溶液血红色变浅 |
11.常温下,物质的量浓度相等的下列溶液pH由大到小的顺序是( )
①Na2CO3②CH3COONa ③CH3CH2ONa ④NH4NO3⑤NaHSO4⑥苯酚钠 ⑦NaHCO3.
①Na2CO3②CH3COONa ③CH3CH2ONa ④NH4NO3⑤NaHSO4⑥苯酚钠 ⑦NaHCO3.
| A. | ③①⑥⑦②④⑤ | B. | ⑥①②⑦③④⑤ | C. | ⑤④③①⑥⑦② | D. | ⑥③⑦①②④⑤ |
10.有关常温下pH均为3的硫酸和醋酸溶液的说法正确的是( )
| A. | 分别加水稀释100倍后,硫酸溶液的pH变化比醋酸溶液小 | |
| B. | 两种溶液中,由水电离出的c(H+)=1×10-11mol•L-1 | |
| C. | 与pH=11的NaOH溶液等体积混合后,都恰好中和 | |
| D. | 分别加入足量锌片充分反应后,两溶液中产生的氢气一样多 |
9.下列方程式中,属于水解反应且书写正确的是( )
| A. | SO32-+H2O?HSO3-+OH- | B. | CO32-+2H2O?H2CO3+2 OH- | ||
| C. | HS-+H2O?H3O++S2- | D. | Al3++3H2O=Al(OH)3↓+3H+ |
8.按电子排布,可把周期表里的元素划分成5个区,以下元素属于p区的是( )
0 157567 157575 157581 157585 157591 157593 157597 157603 157605 157611 157617 157621 157623 157627 157633 157635 157641 157645 157647 157651 157653 157657 157659 157661 157662 157663 157665 157666 157667 157669 157671 157675 157677 157681 157683 157687 157693 157695 157701 157705 157707 157711 157717 157723 157725 157731 157735 157737 157743 157747 157753 157761 203614
| A. | Fe | B. | S | C. | Mg | D. | Cu |