13.下列说法不正确的是( )
| A. | 氧气和臭氧互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$ He和${\;}_{2}^{4}$He互为同位素 | |
| D. | ${\;}_{2}^{4}$ He的最外层电子数为2,所以${\;}_{2}^{3}$He具有较强的金属性 |
12.如表列出了前20号元素中的某些元素性质的一些数据:
(1)以上10种元素中,电负性最大的是O(填元素符号).
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物反应:C+4HNO3(浓)=CO2↑+4NO2↑+2H2O.
②B2C2与EC2反应:2K2O2+2CO2=2K2CO3+O2.
(3)A元素原子核外电子排布图是1s22s22p63s23p4;比元素B原子序数大11的元素的原子的电子排布式是1s22s22p63s23p63d104s2或者[Ar]3d104s2.
(4)C和I相比较,非金属性较弱的是氮(填元素名称).
| 元素 性质 | A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10 m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高 价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低 价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物反应:C+4HNO3(浓)=CO2↑+4NO2↑+2H2O.
②B2C2与EC2反应:2K2O2+2CO2=2K2CO3+O2.
(3)A元素原子核外电子排布图是1s22s22p63s23p4;比元素B原子序数大11的元素的原子的电子排布式是1s22s22p63s23p63d104s2或者[Ar]3d104s2.
(4)C和I相比较,非金属性较弱的是氮(填元素名称).
11.下列晶体中含有非极性共价键的离子晶体是( )
①硅晶体 ②H2O2 ③CaC2 ④NH4Cl ⑤Na2O2 ⑥苯酚.
①硅晶体 ②H2O2 ③CaC2 ④NH4Cl ⑤Na2O2 ⑥苯酚.
| A. | ①②④⑥ | B. | ①③ | C. | ②④⑤⑥ | D. | ③⑤ |
10.第三周期元素中,微粒半径最大的是( )
| A. | Al3+ | B. | Na+ | C. | S2- | D. | Cl- |
4.质谱显示,某有机化合物的相对分子质量为46,燃烧实验发现其分子中碳、氢原子数之比为1:3,核磁共振谱显示,该物质中只有一种类型的氢原子.关于该化合物的描述中,正确的是( )
0 157543 157551 157557 157561 157567 157569 157573 157579 157581 157587 157593 157597 157599 157603 157609 157611 157617 157621 157623 157627 157629 157633 157635 157637 157638 157639 157641 157642 157643 157645 157647 157651 157653 157657 157659 157663 157669 157671 157677 157681 157683 157687 157693 157699 157701 157707 157711 157713 157719 157723 157729 157737 203614
| A. | 该化合物为乙醇 | B. | 该化合物与乙醇互为同分异构体 | ||
| C. | 该化合物为乙醚 | D. | 该化合物与乙醚互为同分异构 |
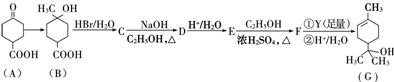
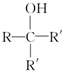 ,请回答下列问题:
,请回答下列问题: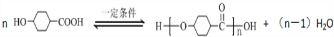 .
. .
. .
. .
.
 .
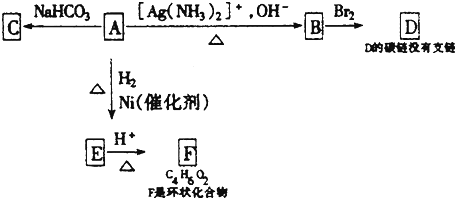
.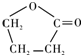 .由E生成F的反应类型是酯化反应.
.由E生成F的反应类型是酯化反应. )是一种重要的化工原料,其合成路线如下:
)是一种重要的化工原料,其合成路线如下: $→_{AlCl_{3}}^{CH_{3}CH=CH_{2}}$
$→_{AlCl_{3}}^{CH_{3}CH=CH_{2}}$ $→_{反应①}^{氯代反应}$[A]$\stackrel{反应②}{→}$
$→_{反应①}^{氯代反应}$[A]$\stackrel{反应②}{→}$ $\stackrel{反应③}{→}$
$\stackrel{反应③}{→}$ $\stackrel{反应④}{→}$[D](Mr=136)$\stackrel{反应⑤}{→}$
$\stackrel{反应④}{→}$[D](Mr=136)$\stackrel{反应⑤}{→}$
 +HCl$\stackrel{一定条件}{→}$
+HCl$\stackrel{一定条件}{→}$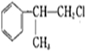 、
、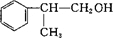 +NaCl.
+NaCl. .
.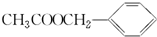 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: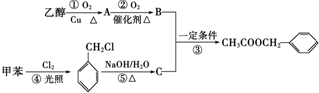
 .
.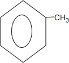 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl.
+HCl.