14.X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物 ZX;Y、M同主族,可形成 MY2、MY3两种分子.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第ⅥA族;
(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式);
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有Cl2、O3
(写出其中两种物质的化学式);
(4)ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑;
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一.元素 E位于第四周期,与元素 Y同主族.在下表中列出对 H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中 E用元素符号表示)
(6)由碳元素(C)、Y和 M三种元素组成的化合物 CYM中,所有原子的最外层满足 8电子结构.写出该化合物的电子式(电子式中 Y、M用元素符号表示)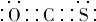 .
.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第ⅥA族;
(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式);
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有Cl2、O3
(写出其中两种物质的化学式);
(4)ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑;
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一.元素 E位于第四周期,与元素 Y同主族.在下表中列出对 H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中 E用元素符号表示)
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2EO3+4HI═Z↓+2I2+3H2O |
| 1 | ||
| 2 |
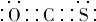 .
.
11.如图中的实验方案,能达到实验目的是( )
| 选项 | A | B | C | D |
| 实验 方案 |  |  |  |  |
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 探究温度对平衡2NO2→N2O4的影响 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
| A. | A | B. | B | C. | C | D. | D |
10.用托盘天平称取10.1g NaOH试样,下列操作中,正确的是( )
| A. | 将NaOH放在天平左边托盘中的纸片上 | |
| B. | 将NaOH放入烧杯中(烧杯事先已称重),并放在天平左边托盘上 | |
| C. | 用镊子取出标定为10.1 g的砝码放在天平右边的托盘上 | |
| D. | 用镊子取出标定为10 g的砝码放在天平左边的托盘上,并将游码向右移到0.1 g位置上 |
9.X、Y、Z、W是元素周期表前四周期中原子序数依次增大的常见元素,其相关信息如表:
(1)Y位于元素周期表第二周期第VA族;Y和Z的氢化物稳定性顺序为:H2O>NH3(写化学式).
(2)X、Y、Z的第一电离能由大到小的顺序为N>O>C;W的基态原子核外电子排布式是1s22s22p63s23p63d64s2(或[Ar]3d64s2)
(3)向W单质与盐酸反应后的溶液中通入过量Y的气态氢化物,能观察到的现象是先出现白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色,发生反应的化学方程式是FeCl2+2NH3.H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(4)已知Y的氢化物在催化加热的条件下,可以与Z2发生氧化还原反应,并且在室温下每转移10mol电子放热akJ,该反应的热化学方程式是4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H=-2akJ.mol-1.
| 元素 | 相关信息 |
| X | X的一种单质是自然界硬度最大的晶体 |
| Y | Y的基态原子最外层电子排布式为nsnnpn+1 |
| Z | Z的基态原子L层电子数是K层电子数的3倍 |
| W | W的一种核素的质量数为58,中子数为32 |
(2)X、Y、Z的第一电离能由大到小的顺序为N>O>C;W的基态原子核外电子排布式是1s22s22p63s23p63d64s2(或[Ar]3d64s2)
(3)向W单质与盐酸反应后的溶液中通入过量Y的气态氢化物,能观察到的现象是先出现白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色,发生反应的化学方程式是FeCl2+2NH3.H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(4)已知Y的氢化物在催化加热的条件下,可以与Z2发生氧化还原反应,并且在室温下每转移10mol电子放热akJ,该反应的热化学方程式是4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H=-2akJ.mol-1.
8.苯乙酸的同分异构体中属于芳香酯的有( )
| A. | 3种 | B. | 5种 | C. | 6种 | D. | 10种 |
7.能正确表示下列反应的离子方程式是( )
0 157531 157539 157545 157549 157555 157557 157561 157567 157569 157575 157581 157585 157587 157591 157597 157599 157605 157609 157611 157615 157617 157621 157623 157625 157626 157627 157629 157630 157631 157633 157635 157639 157641 157645 157647 157651 157657 157659 157665 157669 157671 157675 157681 157687 157689 157695 157699 157701 157707 157711 157717 157725 203614
| A. | AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O | |
| B. | 漂白粉溶液中通入适量的SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| C. | 用稀硝酸除去试管内壁银:3Ag+4H++NO3-=3Ag++NO↑+2H2O | |
| D. | 澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
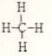 ;X、Z、N形成的原子个数比1:1:1的分子的电子式
;X、Z、N形成的原子个数比1:1:1的分子的电子式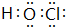 .
.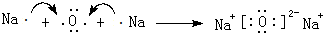 ;
;
 .
. .
.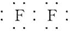 .
.