6.强酸和强碱在稀溶液中的中和热可表示为:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ•mol-1:下面三个热化学方程式
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O (l);△H=-Q1kJ•mol-1
H2SO4(浓)+2NaOH(aq)═Na2SO4(aq)+2H2O(l);△H=-Q2 kJ•mol-1
HNO3(aq)+KOH(aq)═KNO3(aq)+H2O(l);△H=-Q3 kJ•mol-1,
则Q1、Q2、Q3的关系正确的是( )
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O (l);△H=-Q1kJ•mol-1
H2SO4(浓)+2NaOH(aq)═Na2SO4(aq)+2H2O(l);△H=-Q2 kJ•mol-1
HNO3(aq)+KOH(aq)═KNO3(aq)+H2O(l);△H=-Q3 kJ•mol-1,
则Q1、Q2、Q3的关系正确的是( )
| A. | Q1=Q2=Q3 | B. | Q2>Q1>Q3 | C. | Q2>Q3>Q1 | D. | Q2=Q3>Q1 |
4.下列各组物质的反应,有机产物中没有同分异构体的是( )
| A. | CH3CH═CH2与HBr | B. | 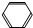 -CH3与混酸(浓HNO3和浓H2SO4,30℃) -CH3与混酸(浓HNO3和浓H2SO4,30℃) | ||
| C. | CH3CH═CHCH3与HBr | D. | 光照条件下CH3CH3与Cl2 |
2.X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)W位于元素周期表第三周期第ⅣA族;W的原子半径比X的大(填“大”或“小”).
(2)Z的第一电离能比W的小(填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是分子间作用力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称乙醇、乙酸等
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是先生成白色沉淀,后沉淀逐渐溶解,最后变成无色溶液;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是Si+4HF=SiF4↑+2H2↑
(4)在25°、101kpa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是2Al(s)+3O2(g)=2Al2O3(s)△H=-3352kJ/mol.
| 元素 | 相关信息 |
| X | X的最高价氧化为对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(2)Z的第一电离能比W的小(填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是分子间作用力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称乙醇、乙酸等
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是先生成白色沉淀,后沉淀逐渐溶解,最后变成无色溶液;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是Si+4HF=SiF4↑+2H2↑
(4)在25°、101kpa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是2Al(s)+3O2(g)=2Al2O3(s)△H=-3352kJ/mol.
1.现有部分元素的原子结构特点如表:
(1)画出W原子结构示意图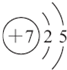 .
.
(2)元素X与元素Z相比,非金属性较强的是O(填元素符号),写出一个能表示X、Z非金属性强弱关系的化学反应方程式S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2或2H2S+O2═2H2O+2S.
(3)X、Y、Z、W四种元素形成的一种化合物,其水溶液显强酸性,该化合物的化学式为NH4HSO4,写出其在水溶液中的电离方程式.NH4HSO4=NH4++H++SO42-
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式.N2H4+2H2O2$\frac{\underline{\;点燃\;}}{\;}$N2+4H2O.
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 共用三对电子形成双原子分子,常温下为气体单质 |
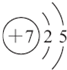 .
.(2)元素X与元素Z相比,非金属性较强的是O(填元素符号),写出一个能表示X、Z非金属性强弱关系的化学反应方程式S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2或2H2S+O2═2H2O+2S.
(3)X、Y、Z、W四种元素形成的一种化合物,其水溶液显强酸性,该化合物的化学式为NH4HSO4,写出其在水溶液中的电离方程式.NH4HSO4=NH4++H++SO42-
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式.N2H4+2H2O2$\frac{\underline{\;点燃\;}}{\;}$N2+4H2O.
19.钠放入盛有空气的密闭容器中生成Na2O和Na2O2,这是下列哪些因素决定的( )
| A. | 反应温度 | B. | 空气的量 | C. | 钠粒的大小 | D. | 钠的状态 |
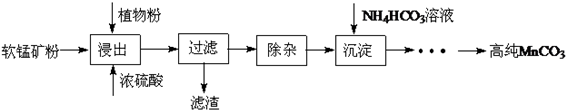
17.科学研究与工业生产中常常用到溶液中的反应.
(1)25℃时,0.05mol•L-1Ba(OH)2溶液的pH=13,将该Ba(OH)2溶液与pH=2的HCl溶液混合,若所得混合溶液pH=7,则Ba(OH)2溶液与HCl溶液的体积比为1:10.
(2)CO2可转化成有机物实现碳循环:CO2$\stackrel{H_{2}}{→}$CH3OH$\stackrel{O_{2}}{→}$HCOOH…
25℃时,几种酸的电离平衡常数如下:
回答下列问题:
①用离子方程式表示HCOONa溶液呈碱性的原因HCOO-+H2O?HCOOH+OH-.
②物质的量浓度均为0.1mol•L-1的下列四种物质:
a.Na2CO3b.NaClO c.HCOONa d.NaHCO3,pH由大到小的顺序是a>b>d>c(填编号).
(3)常温下,将0.2mol•L-1的HCOOH和0.1mol•L-1的NaOH溶液等体积混合,所得溶液的pH<7,说明所得混合溶液中HCOOH的电离程度大于HCOONa的水解程度(填“大于”“等于”或“小于”).
(4)含有Cr2O的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O72-.为使废水能达标排放,做如下处理:Cr2O${\;}_{7}^{2-}$$→_{H+}^{绿矾}$Cr3+、Fe3+$\stackrel{石灰水}{→}$Cr(OH)3、Fe(OH)3.若处理后的废水中残留的c(Fe3+)=2×10-13 mol•L-1,则残留的Cr3+的浓度为3×10-6mol•L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31).
0 157524 157532 157538 157542 157548 157550 157554 157560 157562 157568 157574 157578 157580 157584 157590 157592 157598 157602 157604 157608 157610 157614 157616 157618 157619 157620 157622 157623 157624 157626 157628 157632 157634 157638 157640 157644 157650 157652 157658 157662 157664 157668 157674 157680 157682 157688 157692 157694 157700 157704 157710 157718 203614
(1)25℃时,0.05mol•L-1Ba(OH)2溶液的pH=13,将该Ba(OH)2溶液与pH=2的HCl溶液混合,若所得混合溶液pH=7,则Ba(OH)2溶液与HCl溶液的体积比为1:10.
(2)CO2可转化成有机物实现碳循环:CO2$\stackrel{H_{2}}{→}$CH3OH$\stackrel{O_{2}}{→}$HCOOH…
25℃时,几种酸的电离平衡常数如下:
| 化学式 | HCOOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-4 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
①用离子方程式表示HCOONa溶液呈碱性的原因HCOO-+H2O?HCOOH+OH-.
②物质的量浓度均为0.1mol•L-1的下列四种物质:
a.Na2CO3b.NaClO c.HCOONa d.NaHCO3,pH由大到小的顺序是a>b>d>c(填编号).
(3)常温下,将0.2mol•L-1的HCOOH和0.1mol•L-1的NaOH溶液等体积混合,所得溶液的pH<7,说明所得混合溶液中HCOOH的电离程度大于HCOONa的水解程度(填“大于”“等于”或“小于”).
(4)含有Cr2O的废水毒性较大,某工厂废水中含5.00×10-3 mol•L-1的Cr2O72-.为使废水能达标排放,做如下处理:Cr2O${\;}_{7}^{2-}$$→_{H+}^{绿矾}$Cr3+、Fe3+$\stackrel{石灰水}{→}$Cr(OH)3、Fe(OH)3.若处理后的废水中残留的c(Fe3+)=2×10-13 mol•L-1,则残留的Cr3+的浓度为3×10-6mol•L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31).
 A、B、D、E、F五种元素的原子序数依次增大,除F为过渡元素外,其余四种均是短周期元素.已知:
A、B、D、E、F五种元素的原子序数依次增大,除F为过渡元素外,其余四种均是短周期元素.已知: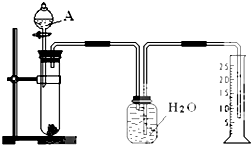 某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数.可供选用的试剂有:浓H2SO4、浓硝酸、6mol•L-1NaOH溶液.请填写下列空白:
某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数.可供选用的试剂有:浓H2SO4、浓硝酸、6mol•L-1NaOH溶液.请填写下列空白: