3.甲烷分子是以C原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )
| A. | CH3Cl只代表一种物质 | B. | CH2Cl2只代表一种物质 | ||
| C. | CHCl3只代表一种物质 | D. | CCl4是非极性分子 |
2.同主族3种元素X、Y、Z,已知它们的最高价氧化物对应水化物的酸性HXO4>HYO4>HZO4则下列判断正确的是( )
| A. | 原子半径X>Y>Z | B. | 气态氢化物稳定性 HX>HZ>HY | ||
| C. | 非金属性X>Y>Z | D. | 气态氢化物还原性HX>HY>HZ |
18.X、Y、Z、W是原子序数依次增大的前四周期常见的元素,其相关信息如表:
(1)W位于元素周期表第四周期第Ⅷ族,其基态原子最外层有2个电子;
(2)X的电负性比Y的小(填“大”或“小”);X和Y的气态氢化物中,较稳定的是H2O(写化学式);
(3)Z元素形成简单离子的离子结构示意图 ;
;
(4)XY2由固态变为气态所需克服的微粒间作用力是范德华力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称是乙酸.
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X的电负性比Y的小(填“大”或“小”);X和Y的气态氢化物中,较稳定的是H2O(写化学式);
(3)Z元素形成简单离子的离子结构示意图
 ;
;(4)XY2由固态变为气态所需克服的微粒间作用力是范德华力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称是乙酸.
16.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是Z元素形成的单质是空气的主要成分之一.已知:甲+乙═丁+己,甲+丙═戊+己; 0.1mol•L-1丁溶液的pH为13(25℃).下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 1 mol甲与足量的乙完全反应共转移了1 mol电子 | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子总的物质的量小于0.1 mol |
14.除去下列杂质(括号内的物质),下列做法不正确的是( )
0 157512 157520 157526 157530 157536 157538 157542 157548 157550 157556 157562 157566 157568 157572 157578 157580 157586 157590 157592 157596 157598 157602 157604 157606 157607 157608 157610 157611 157612 157614 157616 157620 157622 157626 157628 157632 157638 157640 157646 157650 157652 157656 157662 157668 157670 157676 157680 157682 157688 157692 157698 157706 203614
| A. | NaCl固体(CaCl2):溶解,加Na2CO3溶液、过滤后加适量盐酸,最后蒸发结晶 | |
| B. | KCl固体(MnO2):溶解、过滤、蒸发结晶 | |
| C. | NaCl溶液(I2):加酒精,萃取、分液 | |
| D. | KNO3溶液(I2):加四氯化碳,萃取、分液 |
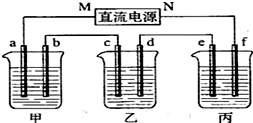
 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二. 无色,无气味并且易燃.是常见的一种化石能源.
无色,无气味并且易燃.是常见的一种化石能源. 有强氧化性的弱酸,见光易分解,具有漂白性,可以用于消毒杀菌.
有强氧化性的弱酸,见光易分解,具有漂白性,可以用于消毒杀菌.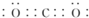 .
.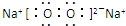 ,AB2所含化学键的类型:离子键、非极性共价键(极性共价键、非极性共价键、离子键).
,AB2所含化学键的类型:离子键、非极性共价键(极性共价键、非极性共价键、离子键).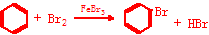 .
.