3.现有部分短周期主族元素的性质或原子结构如表:
(1)元素Y在周期表中的位置第二周期第ⅤA族(周期、族).
(2)XN2的电子式是: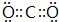 ,Y的简单氢化物的结构式
,Y的简单氢化物的结构式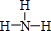 .
.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)用电子式表示WZ的形成过程 .
.
(5)元素Z和T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是B.
A.常温下Z单质和T单质状态不同B.Z的氢化物比T的氢化物稳定
C.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(6)写出W单质和H2O反应的化学方程式2Na+2H2O=2NaOH+H2↑所得溶液的溶质是离子化合物(填“离子”或“共价”).
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大的元素 |
| N | 原子序数比T小,且与T在同一主族 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氨化物的水溶液呈碱性 |
| Z | 元素最高正价为+7价 |
(2)XN2的电子式是:
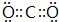 ,Y的简单氢化物的结构式
,Y的简单氢化物的结构式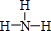 .
.(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)用电子式表示WZ的形成过程
 .
.(5)元素Z和T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是B.
A.常温下Z单质和T单质状态不同B.Z的氢化物比T的氢化物稳定
C.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(6)写出W单质和H2O反应的化学方程式2Na+2H2O=2NaOH+H2↑所得溶液的溶质是离子化合物(填“离子”或“共价”).
2.某科学探究小组为探究电化学原理,设计了如图所示的装置进行探究实验.下列对实验中观察到的现象或有关结论错误的是( )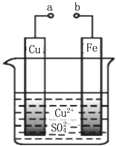

| A. | a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池 | |
| B. | a和b用导线连接时铜片为负极,发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成 | |
| D. | a和b用导线连接时,溶液中的Cu2+应向铜电极移动 |
1.【有机化学】
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味.实验室制备乙酸异戊酯的反应、装置示意图(图1)和有关数据如下:
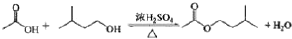
实验步骤:
在A中加入4.4g的异戊醇、6.0g的乙酸、数滴浓硫酸和2~3 片碎瓷片.开始缓慢加热A.回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静里片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B 的名称是球形冷凝管.
(2)在洗涤操作中.第一次水洗的主要目的是洗掉大部分硫酸和醋酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(3)在洗涤、分液操作中,应充分振荡.然后静置,待分层后D(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出.再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口例出
(4)本实验中加入过量乙酸的目的是提高醇的转化率.
(5)实验中加入少量无水MgSO4的目的是干燥乙酸异戊酯.
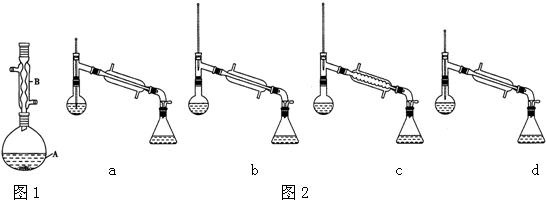
(6)在蒸馏操作中,仪器选择及安装都正确的是图2中b(填标号).
(7)本实验的产率是c(填标号).
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”)
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味.实验室制备乙酸异戊酯的反应、装置示意图(图1)和有关数据如下:
| 相对原子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊醇 | 130 | 0.8670 | 142 | 难溶 |
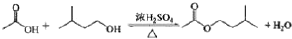
实验步骤:
在A中加入4.4g的异戊醇、6.0g的乙酸、数滴浓硫酸和2~3 片碎瓷片.开始缓慢加热A.回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静里片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B 的名称是球形冷凝管.
(2)在洗涤操作中.第一次水洗的主要目的是洗掉大部分硫酸和醋酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(3)在洗涤、分液操作中,应充分振荡.然后静置,待分层后D(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出.再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口例出
(4)本实验中加入过量乙酸的目的是提高醇的转化率.
(5)实验中加入少量无水MgSO4的目的是干燥乙酸异戊酯.
(6)在蒸馏操作中,仪器选择及安装都正确的是图2中b(填标号).

(7)本实验的产率是c(填标号).
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”)
20.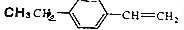 分子中,处于同一平面上的碳原子数最多可能是( )
分子中,处于同一平面上的碳原子数最多可能是( )
 分子中,处于同一平面上的碳原子数最多可能是( )
分子中,处于同一平面上的碳原子数最多可能是( )| A. | 8个 | B. | 9个 | C. | 10个 | D. | 7个 |
18.下列事实不能说明醋酸是弱酸的是( )
| A. | 室温下CH3COONa溶液的pH值大于7 | |
| B. | 同温同浓度的盐酸与CH3COOH溶液比较,醋酸溶液导电能力弱 | |
| C. | CH3COOH不与NaCl反应 | |
| D. | 室温下0.1 mol/L CH3COOH溶液的pH=2.9 |
17.下列表示式中,正确的是( )
| A. | 醋酸的电离方程式:CH3COOH→CH3COO一+H+ | |
| B. | 常温下NH4Cl溶液的pH<7 | |
| C. | 因为SO3的水溶液能够导电,所以SO3是强电解质 | |
| D. | 在常温下的NaOH溶液中,由于NaOH抑制了水的电离,水的离子积常数(KW)减小 |
16.如图为铜锌原电池示意图,下列说法中不正确的是( )


| A. | 锌片逐渐溶解,铜片上有气泡 | B. | 锌片为正极,铜片为负极 | ||
| C. | 电子由锌片通过导线流向铜片 | D. | 该装置能够将化学能转化为电能 |
15.下列各物质间的反应,生成的盐不止一种的是( )
| A. | 氧化铁与稀盐酸 | B. | 铜与浓硫酸 | ||
| C. | 钠在氯气中燃烧 | D. | 氯气通入烧碱溶液 |
14.石油分馏塔装置示意如图.a、b、c分别为石油分馏产品.下列说法正确的是( )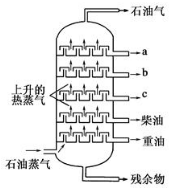
0 157510 157518 157524 157528 157534 157536 157540 157546 157548 157554 157560 157564 157566 157570 157576 157578 157584 157588 157590 157594 157596 157600 157602 157604 157605 157606 157608 157609 157610 157612 157614 157618 157620 157624 157626 157630 157636 157638 157644 157648 157650 157654 157660 157666 157668 157674 157678 157680 157686 157690 157696 157704 203614

| A. | 在a、b、c三种馏分中,a的熔点最高 | |
| B. | 分馏产品的沸点:a>b>c>柴油>重油 | |
| C. | 在a、b、c三种馏分中,c的平均相对分子质量最大 | |
| D. | a、b、c、柴油、重油都是纯净物 |
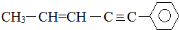 分子结构中在同一平面上的碳原子数最多为11个.
分子结构中在同一平面上的碳原子数最多为11个.