3.根据如表有机物的排列规律可判断,物质X的同分异构体中能与金属钠反应的(不考虑立体异构)共有( )
| 1 | 2 | 3 | 4 | 5 | 6 | … |
| CH4O | C2H6O | C3H8O | x | C5H12O | C6H14O | … |
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
2.下列关于钠元素的几种表达式错误的是( )
| A. | Na+的电子排布图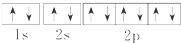 | B. | Na+的结构示意图: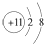 | ||
| C. | Na的电子排布式:1s22s22p63s1 | D. | Na的简化的电子排布式:[Na]3s1 |
20.根据下列热化学方程式,判断氢化物的稳定性顺序正确的是( )
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ•mol-1
I2(g)+H2(g)═2HI(g)△H=-9.4kJ•mol-1.
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ•mol-1
I2(g)+H2(g)═2HI(g)△H=-9.4kJ•mol-1.
| A. | HCl>NH3>HI | B. | HI>HCl>NH3 | C. | HCl>HI>NH3 | D. | NH3>HI>HCl |
17.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A. | X、Z、Y、W的原子半径依次减小 | |
| B. | 若W与Y的原子序数相差5,则二者形成化合物的化学式可能为Y3W2 | |
| C. | W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 | |
| D. | W与X形成的化合物只含离子键 |
16.某化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中三次检验结果如下表所示,请回答下列问题.
(1)三次检验结果中第二次检验结果不正确.
(2)为了确定NH4+的存在,写出鉴定NH4+的实验方法和现象:取原溶液少许,加入浓NaOH溶液,微热,产生的气体能使湿润石蕊的红色石蕊试纸变蓝.
| 检验次数 | 溶液中检验出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NH4Cl |
| 第二次 | NH4Cl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、NH4Cl、K2CO3、NaCl |
(2)为了确定NH4+的存在,写出鉴定NH4+的实验方法和现象:取原溶液少许,加入浓NaOH溶液,微热,产生的气体能使湿润石蕊的红色石蕊试纸变蓝.
15.根据表1信息,判断以下叙述正确的是( )
表1 部分短周期元素的原子半径及主要化合价
0 157506 157514 157520 157524 157530 157532 157536 157542 157544 157550 157556 157560 157562 157566 157572 157574 157580 157584 157586 157590 157592 157596 157598 157600 157601 157602 157604 157605 157606 157608 157610 157614 157616 157620 157622 157626 157632 157634 157640 157644 157646 157650 157656 157662 157664 157670 157674 157676 157682 157686 157692 157700 203614
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L2+与R2-的核外电子数相等 | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T形成的化合物具有两性 | D. | 氢化物的沸点为H2T<H2R |
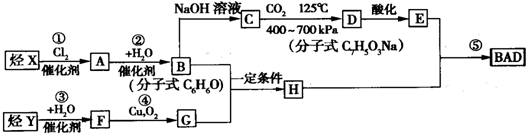

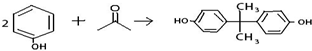
 .
. ;
;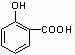 +
+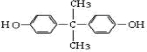 →
→ 三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到.
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到.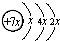 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题: .
. A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.