12.X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如表
(1)Q元素基态原子的电子排布式是1s22s22p63s23p63d64s2,Y原子的电子排布图是 .
.
(2)比较Y元素与氧元素的第一电离能N>O;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是CS2,分子中的 键和π键数目之比为1:1.
键和π键数目之比为1:1.
(3)写出实验室制备M单质的离子方程式MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是HF>HCl,其原因是因为元素非金属性F>Cl,所以HF稳定;
沸点高的是HF>HCl,其原因是因为HF分子之间存在氢键,所以HF沸点高.
| 元素 | 结构或性质信息 |
| X | 其原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M | 单质在常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
| Q | 其与X形成的合金为目前用量最多的金属材料 |
 .
.(2)比较Y元素与氧元素的第一电离能N>O;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是CS2,分子中的
 键和π键数目之比为1:1.
键和π键数目之比为1:1.(3)写出实验室制备M单质的离子方程式MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是HF>HCl,其原因是因为元素非金属性F>Cl,所以HF稳定;
沸点高的是HF>HCl,其原因是因为HF分子之间存在氢键,所以HF沸点高.
11.固体粉末甲由FeSO4、Fe2(SO4)3、CuSO4、CaCO3、SiO2、NaCl中的若干种组成,取一定量的固体甲进行如下实验:

固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g.则下列说法正确的是( )

固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g.则下列说法正确的是( )
| A. | 溶液1加入KSCN溶液一定呈红色 | |
| B. | 取少量溶液2加入酸化的硝酸银溶液,生成白色沉淀,则甲中一定有NaCl | |
| C. | 固体1与稀盐酸反应时还生成了标准状况下气体1.12L | |
| D. | 沉淀2不溶于任何酸溶液 |
9.有X、Y、Z、W、M五种原子序数依次增大的短周期元素,其中X、M同主族;Z+与Y2-具有相同的电子层结构,W是地壳中含量最多的金属,X与W的原子序数之和等于Y与Z的原子序数之和.下列说法不正确的是( )
| A. | 离子半径大小:r(Y 2-)>r(Z +)>r(W 3+) | |
| B. | W的氧化物对应的水化物可能与Z的最高价氧化物的水化物反应 | |
| C. | X有多种同素异形体,而Y不存在同素异形体 | |
| D. | X、M均能与氯形成由极性键构成的正四面体非极性分子 |
8.下列化合物中的所有碳原子都一定在同一平面上的是( )
| A. | CH3(CH2)4CH3 | B. | CH3CH2CHO | C. | CH3CH=CHCH3 | D. | (CH3)3C-C≡C-CH3 |
7.下列有机物既能发生加成反应,又能发生消去反应的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
6.下列化合物的核磁共振氢谱中出现一组峰的是( )
0 157505 157513 157519 157523 157529 157531 157535 157541 157543 157549 157555 157559 157561 157565 157571 157573 157579 157583 157585 157589 157591 157595 157597 157599 157600 157601 157603 157604 157605 157607 157609 157613 157615 157619 157621 157625 157631 157633 157639 157643 157645 157649 157655 157661 157663 157669 157673 157675 157681 157685 157691 157699 203614
| A. | 2,2,3,3一四甲基丁烷 | B. | 2,3,4一三甲基戊烷 | ||
| C. | 3,4一二甲基己烷 | D. | 2,5一二甲基己烷 |
 和
和 ;⑦
;⑦ 和
和 ;
;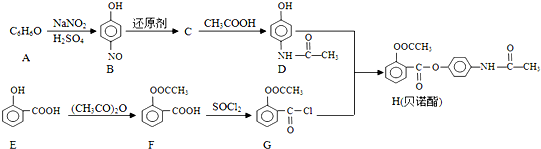
 ;E中含氧官能团的名称为羟基、羧基.
;E中含氧官能团的名称为羟基、羧基. .
. .
.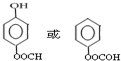 .
.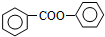 的合成路线流程图(无机试剂可任选):
的合成路线流程图(无机试剂可任选):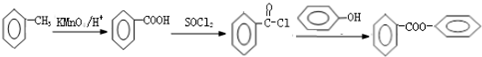 .
.