20.某元素Y的核外电子数等于核内中子数,取2.8g该元素的单质与氧气充分反应,可得6.0g化合物YO2,则该元素在周期表中位置( )
| A. | 第三周期 | B. | 第一周期 | C. | 第ⅤA族 | D. | 第ⅥA族 |
18.己知:KI溶液在酸性条件下能被空气中的O2氧化,反应的离子方程式为:O2+4I-+4H+═2I2+2H2O.
(I)某化学小组为探究不同条件对上述反应速率的影响,设计如下实验,完成表中①和②的内容.
(限选试剂:0.lmol/L硫酸、0.2mol/L硫酸、1mol/L KOH溶液、淀粉溶液)
(2)在上述实验中,三种溶液混合的顺序最合理的是C(选填下列选项);应记录的内容溶液从无色变为蓝色所需的时间.
A.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
B.先将KI溶液与硫酸溶液混合,然后再加入淀粉溶液
C.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
(3)在实验中,发现露置在空气中的KI溶液逐渐变黄色.通过查阅资料知:KI溶液在空气中会生成I2和KOH.小组同学对该描述有疑问:I2为何能与KOH共存?为此提出下列假设进行探究:
假设一:常温下,I2和KOH不反应
假设二:溶液碱性弱,I2和KOH不反应
假设三:…
请设计实验验证假设二,完成表中的内容
(限选试剂:1mol/L盐酸、1mol/L KOH溶液、碘水、淀粉溶液)
(I)某化学小组为探究不同条件对上述反应速率的影响,设计如下实验,完成表中①和②的内容.
(限选试剂:0.lmol/L硫酸、0.2mol/L硫酸、1mol/L KOH溶液、淀粉溶液)
| 组别 | 温度 | KI溶液 | H2SO4溶液 | 淀粉溶液 | 实验目的 | ||
| c(KI) | V | c(H2SO4) | V | ||||
| 1 | 298K | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | 1组和2组探究②0.2mol/L温度对该反应速率的影响;1组和3组探究反应物浓度对该反应速率的影响 |
| 2 | 308K | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | |
| 3 | 298K | 1mol/L | 5mL | ① | 5mL | 3滴 | |
A.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
B.先将KI溶液与硫酸溶液混合,然后再加入淀粉溶液
C.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
(3)在实验中,发现露置在空气中的KI溶液逐渐变黄色.通过查阅资料知:KI溶液在空气中会生成I2和KOH.小组同学对该描述有疑问:I2为何能与KOH共存?为此提出下列假设进行探究:
假设一:常温下,I2和KOH不反应
假设二:溶液碱性弱,I2和KOH不反应
假设三:…
请设计实验验证假设二,完成表中的内容
| 实验方案 | 预期实验现象与结论 |
| 取少量碘水于试管中,滴入几滴淀粉溶液,然后逐滴加入1mol/LKOH溶液,观察现象 | 若蓝色不褪色,则假设二正确 |
17.下列各组气体中均能造成大气污染的是( )
| A. | CO2、O2 | B. | N2、CO | C. | Cl2、N2 | D. | H2S、SO2 |
16.下列有关说法错误的是( )
| A. | X-衍射实验可以区分晶体和非晶体 | B. | SiO2属于原子晶体 | ||
| C. | 金属钋是简单立方堆积 | D. | 晶格能的大小只与离子半径有关 |
11.下列溶液中Cl-浓度与50mL 1mol•L-1 AlCl3溶液中Cl-的物质的量浓度相等的是( )
0 157485 157493 157499 157503 157509 157511 157515 157521 157523 157529 157535 157539 157541 157545 157551 157553 157559 157563 157565 157569 157571 157575 157577 157579 157580 157581 157583 157584 157585 157587 157589 157593 157595 157599 157601 157605 157611 157613 157619 157623 157625 157629 157635 157641 157643 157649 157653 157655 157661 157665 157671 157679 203614
| A. | 150 mL 1 mol•L-1的NaCl溶液 | B. | 75 mL 2 mol•L-1 NH4Cl溶液 | ||
| C. | 150 mL 3 mol•L-1的KCl溶液 | D. | 75 mL 3 mol•L-1的FeCl3溶液 |
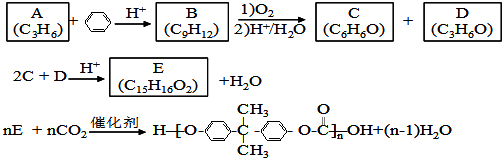
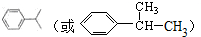 ;
;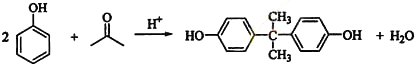 ;
;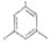 (写出结构简式).
(写出结构简式).
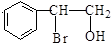 ,F分子中含有的含氧官能团名称是羟基、羧基(顺序可以颠倒).
,F分子中含有的含氧官能团名称是羟基、羧基(顺序可以颠倒). .
.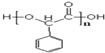 .
.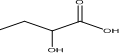 的合成线路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.
的合成线路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.