20.羧酸分子里的官能团是( )
| A. | 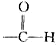 | B. | 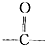 | C. | 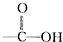 | D. | -CnHn+1 |
19.关于人造丝和蚕丝的叙述不正确的是( )
| A. | 主要成分都是蛋白质 | B. | 都是高分子化合物 | ||
| C. | 可用灼烧的方法区别二者 | D. | 二者成分不同,但燃烧产物相同 |
18.铁在工业和生活中都具有非常重要的应用.某含铁化合物W,为探究其成分,化学兴趣小组的同学取化合物W粉末进行试验.经组成分析,该粉末除Fe外还有O和另一未知元素共三种元素.另取2.22g化合物W的粉末溶于适量稀硫酸,向反应后的溶液中加入含有3.20gNaOH的溶液,恰好完全反应.过滤,将洗涤后的沉淀充分灼烧,得到红棕色粉末1.60g;将所得滤液在一定条件下蒸发灼烧可得到一种纯净的不含结晶水的盐7.10g.请回答:
(1)则另一未知元素为Na(填化学式).
(2)①该化合物W的化学式为NaFeO2.
②该化合物W与适量稀硫酸反应的化学方程式2NaFeO2+4H2SO4=Na2SO4+Fe2(SO4)3+4H2O.
(3)草酸钴是广泛应用于磁性材料、电池材料、及超硬材料等领域.某研究小组在实验室探究CoC2O4分解反应的平衡常数.将一定量纯净的CoC2O4粉末置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解的平衡:CoC2O4(s)?CoO(s)+CO(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
由表中数据,列式计算250℃时CoC2O4分解平衡常数2.89×10-6.该反应的焓变△H>0(填“>”、“=”或“<”).
(4)温度加热至350℃,CO2的体积分数开始发生变化,体积分数和温度的关系如下:
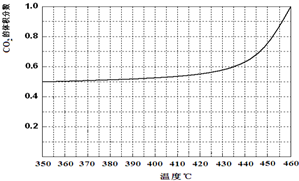
试画出CO的体积分数随温度变化的曲线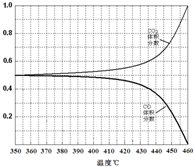 .
.
(1)则另一未知元素为Na(填化学式).
(2)①该化合物W的化学式为NaFeO2.
②该化合物W与适量稀硫酸反应的化学方程式2NaFeO2+4H2SO4=Na2SO4+Fe2(SO4)3+4H2O.
(3)草酸钴是广泛应用于磁性材料、电池材料、及超硬材料等领域.某研究小组在实验室探究CoC2O4分解反应的平衡常数.将一定量纯净的CoC2O4粉末置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解的平衡:CoC2O4(s)?CoO(s)+CO(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 240 | 250 | 260 | 270 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 |
| 平衡气体总浓度/ mol•L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 |
(4)温度加热至350℃,CO2的体积分数开始发生变化,体积分数和温度的关系如下:

试画出CO的体积分数随温度变化的曲线
 .
.
14.下列说法中,错误的是( )
| A. | 元素周期表中,有18个纵行即有18个族 | |
| B. | 最外层电子数为2的元素原子,不一定属于ⅡA族元素 | |
| C. | 在周期表里,元素所在的周期序数等于原子核外的电子层数 | |
| D. | 副族与Ⅷ族元素都是金属元素 |
13.下列说法正确的是( )
| A. | SO2和Cl2使品红溶液褪色的原理相同 | |
| B. | 浓硫酸分别使胆矾变白、蔗糖变黑时,浓硫酸表现的性质相同 | |
| C. | 浓硝酸和浓硫酸露置在空气中,浓度都降低的原因相同 | |
| D. | 浓硫酸与稀硫酸都能与金属锌反应放出气体,两个反应的氧化产物相同 |
12.下列反应中,硫酸既表现出强氧化性,又表现出酸性的是( )
| A. | 稀硫酸与锌粒反应生成气体 | B. | 浓硫酸使铁、铝钝化 | ||
| C. | 浓硫酸与铜反应加热反应产生SO2 | D. | 浓硫酸和木炭在加热条件下反应 |
11.下列说法错误的是( )
0 157479 157487 157493 157497 157503 157505 157509 157515 157517 157523 157529 157533 157535 157539 157545 157547 157553 157557 157559 157563 157565 157569 157571 157573 157574 157575 157577 157578 157579 157581 157583 157587 157589 157593 157595 157599 157605 157607 157613 157617 157619 157623 157629 157635 157637 157643 157647 157649 157655 157659 157665 157673 203614
| A. | 二氧化碳和二氧化硅都属于原子晶体 | |
| B. | 分子晶体的状态变化,只需克服分子间作用力 | |
| C. | 金属晶体通常具有导电、导热性能和良好的延展性 | |
| D. | 离子晶体在熔化状态下能导电 |
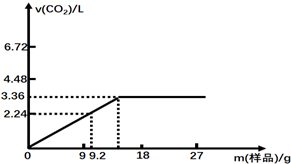
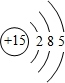
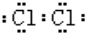
 .
.