8.某品牌的家用消毒剂其有效成分为对氯间二甲苯酚(结构简式如图所示),可以杀灭常见的病毒与细菌.下面有关该物质的说法正确的是( )

| A. | 该物质的分子式是C8H10ClO | |
| B. | 1 mol该物质最多可以与2 mol NaOH反应 | |
| C. | 1 mol该物质可以与2 mol液溴发生取代反应 | |
| D. | 该物质可以发生加成、取代、消去、氧化等反应 |
7.如图中所示的实验方法、装置或操作完全正确的是( )
| A. | 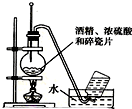 实验室制乙烯 | B. | 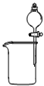 分离苯酚和水 | ||
| C. |  石油的蒸馏 | D. | 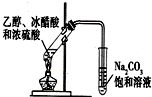 实验室制乙酸乙酯 |
6.下列反应属于取代反应的是( )
| A. | 由乙酸和乙醇制乙酸乙酯 | B. | 由乙醇制乙烯 | ||
| C. | 由丙烯与溴制1,2-二溴丙烷 | D. | 由甲苯氧化制苯甲酸 |
5.如表实验操作与相对应实验目的不正确的是( )
| 实验操作 | 实验目的 | |
| A | C2H4与C2H6混合气体通过盛有酸性KMnO4的洗气瓶 | 除去C2H6中的C2H4 |
| B | 制溴苯时用Fe | 加快化学反应速率 |
| C | 淀粉溶液水解后冷却至室温,加碘水观察现象 | 检验淀粉是否完全水解 |
| D | 将溴乙烷与氢氧化钠水溶液共热一段时间,先加稀硝酸,再向冷却后的混合液中滴加硝酸银溶液 | 检验溴乙烷中的溴原子 |
| A. | A | B. | B | C. | C | D. | D |
4.对有机反应中有机物化学键变化的认识有助于理解有机反应的实质.对下列有机反应中化学键变化的认识不正确的是(“ ”或“
”或“ ”表示化学键断裂处,“
”表示化学键断裂处,“ ”表示生成的化学键( )
”表示生成的化学键( )
 ”或“
”或“ ”表示化学键断裂处,“
”表示化学键断裂处,“ ”表示生成的化学键( )
”表示生成的化学键( )| A. | 乙醇催化氧化: | B. | 乙酸和乙醇的酯化反应: | ||
| C. | 溴乙烷的消去反应: | D. | 乙醛的还原反应: |
3.下列有机反应中,不属于取代反应的是( )
| A. | 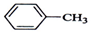 +Cl2$\stackrel{光照}{→}$ +Cl2$\stackrel{光照}{→}$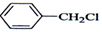 +HCl +HCl | |
| B. | 2CH3CH2+O2$→_{△}^{Cu}$2CH3CHO+2H20 | |
| C. | ClCH2=CH2+NaOH $→_{△}^{H_{2}O}$ HOCH2CH=CH2+NaCl | |
| D. | 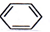 +HONO2 $→_{△}^{浓硫酸}$ +HONO2 $→_{△}^{浓硫酸}$ 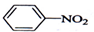 +H2O +H2O |
2.某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳.由此可以得出该有机物的组成必须满足
( )
( )
| A. | 分子中C、H、O的个数比为1:2:3 | B. | 分子中C、H的个数比为1:2 | ||
| C. | 该有机物的分子量为14 | D. | 该分子中肯定不含氧元素 |
1.如图1是某化学兴趣小组设计的利用电子垃圾(含70%Cu、25%Al、4%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线:
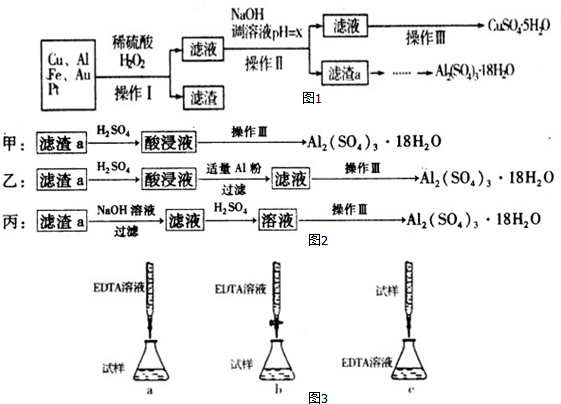
已知下列信息:
Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如表:
请回答下列问题:
(1)操作Ⅰ后,滤渣中有Au、Pt_金属.
(2)写出Cu与稀硫酸和H2O2的混合液反应的离子方程式:Cu+H2O2+2H+=Cu2++2H2O.
(3)在操作Ⅱ中,x的取值范围是5.2≤x<5.4.
(4)由滤渣a制取Al2(SO4)3•l8H2O,探究小组设计了如图2三种方案:综合考虑上述三种方案,最具可行性的是乙(填序号).
(5)为测定CuSO4•5H2O晶体的纯度,进行下列实验:取a g试样配成l00mL溶液,每次取20.00mL,消除干扰离子后,用b mol•L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液l2.00mL.(常温时,5%的Na2H2Y水溶液,其pH为4-6.)
①CuSO4•5H2O晶体的纯度是$\frac{15b}{a}$×100%.
②如图3滴定方式中,最合理的是(夹持部分略去)b(填序号).
0 157446 157454 157460 157464 157470 157472 157476 157482 157484 157490 157496 157500 157502 157506 157512 157514 157520 157524 157526 157530 157532 157536 157538 157540 157541 157542 157544 157545 157546 157548 157550 157554 157556 157560 157562 157566 157572 157574 157580 157584 157586 157590 157596 157602 157604 157610 157614 157616 157622 157626 157632 157640 203614

已知下列信息:
Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |
(1)操作Ⅰ后,滤渣中有Au、Pt_金属.
(2)写出Cu与稀硫酸和H2O2的混合液反应的离子方程式:Cu+H2O2+2H+=Cu2++2H2O.
(3)在操作Ⅱ中,x的取值范围是5.2≤x<5.4.
(4)由滤渣a制取Al2(SO4)3•l8H2O,探究小组设计了如图2三种方案:综合考虑上述三种方案,最具可行性的是乙(填序号).
(5)为测定CuSO4•5H2O晶体的纯度,进行下列实验:取a g试样配成l00mL溶液,每次取20.00mL,消除干扰离子后,用b mol•L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液l2.00mL.(常温时,5%的Na2H2Y水溶液,其pH为4-6.)
①CuSO4•5H2O晶体的纯度是$\frac{15b}{a}$×100%.
②如图3滴定方式中,最合理的是(夹持部分略去)b(填序号).
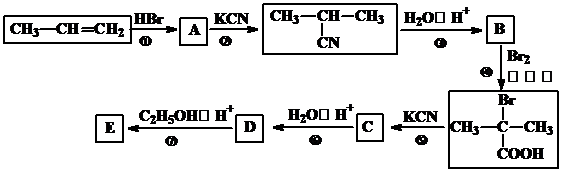
 ;
; +2C2H5OH$→_{△}^{浓硫酸}$
+2C2H5OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.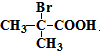 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为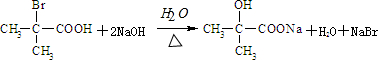 .
. 、
、 .
.