9.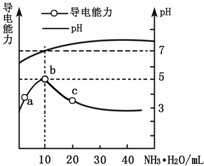 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )
 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )| A. | b点溶液pH=5,此时酸碱恰好中和 | |
| B. | a~b点导电能力增强,说明HR为弱酸 | |
| C. | c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | |
| D. | b~c任意点溶液均有c(H+)•c(OH-)=KW=1.0×10-14 |
8.氢氯混和气体在光照条件下会发生爆炸.在反应过程中,假设破坏1mol氢气中的化学键需要消耗的能量为Q1kJ,破坏1mol氯气中的化学键需要消耗的能量为Q2kJ,形成1mol氯化氢会释放出Q3kJ的能量.下列关系正确的是( )
| A. | Q1+Q2>Q3 | B. | Q1+Q2<Q3 | C. | Q1+Q2>2Q3 | D. | Q1+Q2<2Q3 |
4.需要加入氧化剂才能实现下列反应的是( )
| A. | Zn-→Zn2+ | B. | H+-→H2 | C. | MnO2-→Mn2+ | D. | Cl2-→Cl- |
3.在标准状况下,11.2L H2的物质的量为( )
| A. | 1mol | B. | 2mol | C. | 0.5mol | D. | 1.5mol |
2.下列叙述正确的是( )
| A. | 对于反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,若使用催化剂,反应过程中放出的热量更多 | |
| B. | CO燃烧的热化学方程式为2CO(g)+O2(g)=2CO2(g)△H=+285.8kJ/mol | |
| C. | 反应2Mg+CO2=2MgO+C△H<0从熵变角度看,不可自发进行 | |
| D. | 在密闭容器中,2HI(g)?H2(g)+I2(g)△H=+14.9kJ/mol,若投入NA个HI分子,反应平衡时,吸热7.45kJ |
1.已知:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ•mol-1.现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol•L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2和△H3的大小关系为( )
0 157444 157452 157458 157462 157468 157470 157474 157480 157482 157488 157494 157498 157500 157504 157510 157512 157518 157522 157524 157528 157530 157534 157536 157538 157539 157540 157542 157543 157544 157546 157548 157552 157554 157558 157560 157564 157570 157572 157578 157582 157584 157588 157594 157600 157602 157608 157612 157614 157620 157624 157630 157638 203614
| A. | △H1=△H2>△H3 | B. | △H3>△H1>△H2 | C. | △H3>△H2>△H1 | D. | △H2>△H1>△H3 |
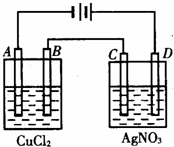 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: