A.移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞 |
B.用标准溶液润洗滴定管2-3次 |
C.把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液 |
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm |
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)B-
(2)滴定开始后,眼睛注视 ,判断到达终点的现象是 。
(3)下列操作中可能使所测盐酸的浓度数值偏高的是
A 碱式滴定管未用标准溶液润洗就直接注入标准液
B 滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留
C 碱式滴定管在滴定前有气泡,滴定后气泡消失
D 读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数
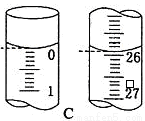
(4)滴定开始和结束时,碱式滴定管中的液面如图C所示,则终点读数为 mL,所测盐酸溶液的浓度为 mol/L。
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
0 157438 157446 157452 157456 157462 157464 157468 157474 157476 157482 157488 157492 157494 157498 157504 157506 157512 157516 157518 157522 157524 157528 157530 157532 157533 157534 157536 157537 157538 157540 157542 157546 157548 157552 157554 157558 157564 157566 157572 157576 157578 157582 157588 157594 157596 157602 157606 157608 157614 157618 157624 157632 203614
| A. | 在相同温度下,pH=1且体积为1L的硫酸溶液所含的H+数与pH=13且体积为1L的氢氧化钠溶液所含的OH-数一定均为0.1NA | |
| B. | 7.8gNa2S和Na2O2的混合物中所含离子数为0.3NA | |
| C. | 在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2,转移的电子数为8NA | |
| D. | 在标准状况下,2.24LHF中含有的电子数为NA |
 2NO2△H>0)
2NO2△H>0)
 。恒容时,温度升高,H2浓度减小,下列说法正确的是
。恒容时,温度升高,H2浓度减小,下列说法正确的是 CO2+H2
CO2+H2 C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则 2SO3(g) △H<0
2SO3(g) △H<0
 CO(g)+H2(g) ΔH=+131.3KJ/mol,反应的平衡常数表达式为K= 。
CO(g)+H2(g) ΔH=+131.3KJ/mol,反应的平衡常数表达式为K= 。