12.某溶液中有Fe3+、Mg2+、Fe2+和Al3+四种阳离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子组合是( )
| A. | Mg2+ | B. | Mg2+、Fe2+ | C. | Fe2+ | D. | Mg2+、Al3+ |
9.“绿色化学”是21世纪化学发展的主要方向.“绿色化学”要求从根本上消除污染,它包括“原料的绿色化”、“化学反应的绿色化”、“产物的绿色化”等内容.其中“化学反应的绿色化”要求反应物中所有的原子完全被利用且全部转入期望的产品中.下列符合“化学反应的绿色化”的是( )
| A. | SO2+2NH3+H2O═(NH4)2SO3 | |
| B. | NO2+NO+2NaOH═2NaNO2+H2O | |
| C. | Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O | |
| D. | CuO+H2SO4(稀)═CuSO4+H2O |
7.下列反应中,属于取代反应的是( )
| A. | 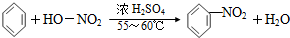 | |
| B. |  | |
| C. | 2 CH3CH2OH+O2 $→_{△}^{催化剂}$ 2 CH3CHO+2 H2O | |
| D. | CH2=CH2+HCl→CH3CH2Cl |
6.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示: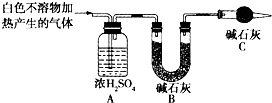
称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 ;
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为 ①氢气 |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量 ②稀盐酸 | ③产生气泡沉淀全部溶解 | 白色不溶物可能含有猜测2中不溶物 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在 ④CO32- |

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 ;
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行.
4.X、Y、Z、W代表短周期的四种元素,有关它们的部分信息如表所示:
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答,请用相应的元素符号或化学式填写):
(1)X的元素名称是,X的气态氢化物的电子式是 .
.
(2)Z元素在周期表中的位置是第三周期,第ⅦA族.Z和W形成的化合物属于共价化合物(填“离子”或“共价”).
(3)X、Y、Z、W的原子半径从大到小的顺序是Al>Cl>C>N.
(4)X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是:HClO4>HNO3>H2CO3.
(5)铜和X的最高价氧化物的水化物的浓溶液反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
(6)气体分子(YX)2称为拟卤素,性质与卤素类似,请写出(YX)2与NaOH溶液反应的化学方程式:(CN)2+2NaOH=NaCN+NaCNO+H2O.
0 157432 157440 157446 157450 157456 157458 157462 157468 157470 157476 157482 157486 157488 157492 157498 157500 157506 157510 157512 157516 157518 157522 157524 157526 157527 157528 157530 157531 157532 157534 157536 157540 157542 157546 157548 157552 157558 157560 157566 157570 157572 157576 157582 157588 157590 157596 157600 157602 157608 157612 157618 157626 203614
| 元素 | 部分结构特点 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14 个电子 | X有多种氧化物,如XO、XO2等 |
| Y | Y原子的次外层电子数等于最外层电子数 的一半 | Y元素能形成多种单质 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价的代数和等于6 |
| W | 第三周期元素的简单离子中半径最小 | W的单质化学性质虽较活泼,但只需常温保存 |
(1)X的元素名称是,X的气态氢化物的电子式是
 .
.(2)Z元素在周期表中的位置是第三周期,第ⅦA族.Z和W形成的化合物属于共价化合物(填“离子”或“共价”).
(3)X、Y、Z、W的原子半径从大到小的顺序是Al>Cl>C>N.
(4)X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是:HClO4>HNO3>H2CO3.
(5)铜和X的最高价氧化物的水化物的浓溶液反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
(6)气体分子(YX)2称为拟卤素,性质与卤素类似,请写出(YX)2与NaOH溶液反应的化学方程式:(CN)2+2NaOH=NaCN+NaCNO+H2O.
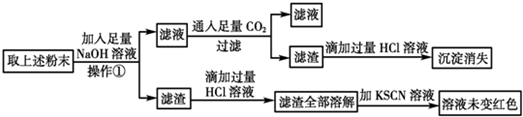
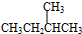 与
与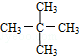 G.
G.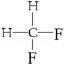 与
与 
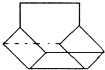
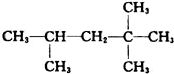 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:CH3C(CH3)2C(CH3)2CH3;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:CH3C(CH3)2C(CH3)2CH3;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为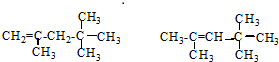 .
.
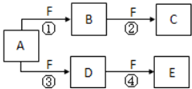 X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示:
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示: .
. ①~⑧是元素周期表中前四周期的8种元素,其相对位置如图所示.
①~⑧是元素周期表中前四周期的8种元素,其相对位置如图所示. .
.