2.在80g密度为d g/cm3的硫酸铁溶液中,含有2.8g Fe3+离子,则此溶液中SO42-的物质的量浓度为(单位为 mol•L-1)( )
| A. | $\frac{15d}{16}$ | B. | 165d | C. | 83d | D. | 85d |
1.用如图装置能达到有关实验目的是( )
| A. |  电解精炼铝 | B. | 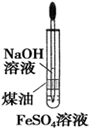 制备Fe(OH)3 | ||
| C. | 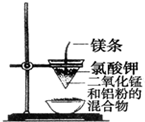 可制得金属锰 | D. | 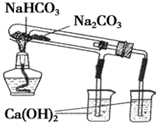 验证NaHCO3和Na2CO3的热稳定性 |
20. 如图是元素周期表的一部分.表中所列字母分别代表某一化学元素.
如图是元素周期表的一部分.表中所列字母分别代表某一化学元素.
(1)下列④(填写编号)组元素的单质具有良好导电性.
①a、c、m ②b、g、k ③c、h、1 ④d、e、f
(2)电离能主要取决于原子核对核外电子的吸引力和形成稳定结构的倾向.如表是一些气态原子各级电离能的数据(kJ•mol-1):
①为什么锂原子的第二电离能远远大于第一电离能最外层电子排布为1S2,轨道全满.
②用电子式表示X和j以原子个数1比1形成的一种化合物 .
.
③Y在周期表中是ⅢA族元素.
④e 元素的电子排布式为1s22s22p63s23p63d24s2.
 如图是元素周期表的一部分.表中所列字母分别代表某一化学元素.
如图是元素周期表的一部分.表中所列字母分别代表某一化学元素.(1)下列④(填写编号)组元素的单质具有良好导电性.
①a、c、m ②b、g、k ③c、h、1 ④d、e、f
(2)电离能主要取决于原子核对核外电子的吸引力和形成稳定结构的倾向.如表是一些气态原子各级电离能的数据(kJ•mol-1):
| 锂 | X | Y | |
| 失去一个电子 | 519 | 502 | 580 |
| 失去二个电子 | 7296 | 4570 | 1820 |
| 失去三个电子 | 11799 | 6920 | 2750 |
| 失去四个电子 | 9550 | 11600 |
②用电子式表示X和j以原子个数1比1形成的一种化合物
 .
.③Y在周期表中是ⅢA族元素.
④e 元素的电子排布式为1s22s22p63s23p63d24s2.
19.下列对极性分子和非极性分子的认识正确的是( )
| A. | 含非极性键的分子一定是非极性分子 | |
| B. | 含有极性键的分子一定是极性分子 | |
| C. | 双原子极性分子一定含有极性键 | |
| D. | 非极性分子一定含有非极性键 |
18.下列叙述中,错误的是( )
| A. | 离子化合物中可能含有非极性键 | B. | 分子晶体中的分子内不含有离子键 | ||
| C. | 原子晶体中可能含有非极性键 | D. | 分子晶体中的分子内一定有共价键 |
17.下列物质的分子中,只由σ键形成的是( )
| A. | 氮气 | B. | 甲烷 | C. | 乙烯 | D. | 乙炔 |
16.下列晶体熔化时不需破坏化学键的是( )
| A. | 晶体硅 | B. | 食盐 | C. | 固体碘 | D. | 金属钾 |
15.下列说法不正确的是( )
| A. | 互为同系物的有机物其组成元素相同,且结构必须相似 | |
| B. | 正戊烷分子中所有碳原子均在一条直线上 | |
| C. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| D. | 互为同系物的有机物其相对分子质量数值一定相差14 n(n为正整数) |
14.已知1-18号元素的离子aW3+、b X+、CY2-、d Z- 都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A. | 四种元素位于同一周期 | B. | 氢化物的稳定性H2Y>HZ | ||
| C. | 离子的氧化性aW3+>bX+ | D. | 原子序数:c>b |
13.在已处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明平衡移动的是( )
0 157419 157427 157433 157437 157443 157445 157449 157455 157457 157463 157469 157473 157475 157479 157485 157487 157493 157497 157499 157503 157505 157509 157511 157513 157514 157515 157517 157518 157519 157521 157523 157527 157529 157533 157535 157539 157545 157547 157553 157557 157559 157563 157569 157575 157577 157583 157587 157589 157595 157599 157605 157613 203614
| A. | 反应混和物各组分的浓度 | B. | 反应物的转化率 | ||
| C. | 正、逆反应速率 | D. | 反应混和物的压强 |