11.关于可逆反应X2(g)+3Y2(g)?2XY3(g)△H<0,下列叙述正确的是( )
| A. | 降低温度可以缩短反应达到平衡的时间 | |
| B. | 恒容时通入氩气,压强增大,平衡向右移动 | |
| C. | 恒容时通入X2,平衡向正反应方向移动,平衡常数不变 | |
| D. | 恒温恒压下,若混合气体密度不变,说明反应已达平衡 |
10.在一密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g)?N2(g)+2CO2(g);△H=-373.2kJ/mol,达到平衡后,为提高NO的转化率,采取的正确措施是( )
| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 | ||
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |
9.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 14 g乙烯和丙烯混合气体中的氢原子数为2NA | |
| B. | 1 molN2与4 mol H2反应生成的NH3分子数为2NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 标准状况下,2.24 LCCl4含有的共价键数为0.4NA |
5.下列实验能获得成功的是( )
| A. | 苯和液溴用溴化铁作催化剂生成溴苯 | |
| B. | 向苯酚浓溶液中滴入少量浓溴水可观察到白色三溴苯酚沉淀 | |
| C. | 银氨溶液配制后加入稀硝酸使溶液呈酸性,再滴入乙醛溶液共热,有银镜生成 | |
| D. | 加氢氧化钠钠溶液,充分振荡,分液可除去乙酸乙酯中的乙酸 |
4.已知过氧乙酸(CH3COOOH)与H2O2存在如下反应:CH3COOH+H2O2?CH3COOOH+H2O,下列有关说法正确的是( )
| A. | 降低温度可加快该反应速率 | |
| B. | 加入合适的催化剂可提高该反应速率 | |
| C. | 达到平衡时,v(正)=v(逆)=0 | |
| D. | 达到平衡时,H2O2转化率为100% |
3.工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g)△H=+Q kJ•mol-1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
0 157416 157424 157430 157434 157440 157442 157446 157452 157454 157460 157466 157470 157472 157476 157482 157484 157490 157494 157496 157500 157502 157506 157508 157510 157511 157512 157514 157515 157516 157518 157520 157524 157526 157530 157532 157536 157542 157544 157550 157554 157556 157560 157566 157572 157574 157580 157584 157586 157592 157596 157602 157610 203614
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ | |
| C. | 反应至4 min时,若HCl浓度为0.12 mol•L-1,则H2的反应速率为0.03 mol•(L•min-1) | |
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol•L-1的NaOH溶液中恰好反应 |
 已知尿素(结构简式:
已知尿素(结构简式: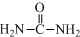 )可用于制有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.回答下列问题.
)可用于制有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.回答下列问题. 碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题:
碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题: