5.某溶液加入金属铝能放出氢气.下列各组离子在该溶液中一定可以大量共存的是( )
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、Cl-、SO42-、HCO3- | ||
| C. | Na+、CH3COO-、NO3-、K+ | D. | K+、Na+、Cl-、SO42- |
4.下列说法中,错误的是(( )
| A. | 浓硫酸常见的特性是吸水性、脱水性、氧化性 | |
| B. | 浓硫酸也具有酸性,在常温下能够与活泼金属铁、铝等反应放出氢气 | |
| C. | 氟化氢的热稳定性很好,具有极弱的还原性,为一元弱酸 | |
| D. | SO2、SO3都是酸性氧化物,具有酸性氧化物的通性 |
3.下列材料的特性及用途说法错误的是(( )
| A. | 高纯硅用于制造光导纤维,实现光电信号转化 | |
| B. | 石英中无色透明的晶体就是通常所说的水晶,其主要成分是二氧化硅 | |
| C. | 光导纤维导光的能力很强,是非常好的通讯材料 | |
| D. | 硅胶多孔,吸附水能力强,可以用作催化剂的载体 |
2.下列物质中,长期露置在空气中,不会变质的是( )
| A. | 硫酸亚铁 | B. | 氯水 | C. | 食盐 | D. | 漂白粉 |
20. (1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
(1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
已知反应①中相关的化学键键能数据如表:
由此计算△H1=-99kJ•mol-1.已知△H2=-58kJ•mol-1,则△H3=+41kJ•mol-1.
 (1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
(1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
已知反应①中相关的化学键键能数据如表:
| 化学键 | H-H | C-O | C-O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1075 | 465 | 413 |
19. 研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ
CO2(g)+H2(g)?CO(g)+H2O(g)△H2=+41.2kJ•mol-8平衡常数K2 反应Ⅱ
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如表实验数据:
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性;转化的CO2中生成甲醇的百分比
(1)合成的甲醇可用于燃料电池的燃料,若电解质为稀烧碱溶液时甲醇燃料电池的正极反应式为O2+4e-+2H2O=4OH-;研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在阴极,该电极反应式是CO2+6e-+6H+=CH3OH+H2O.
(2)从表中实验数据可以分析出,提高CO2转化成CH3OH的选择性的方法有使用Cat2催化剂(或理想催化剂);温度为543K(或降低温度).
(3)反应CO(g)+2H2(g)?CH3OH(g)的平衡常数K3=$\frac{{K}_{1}}{{K}_{2}}$(用K1和K2表示).
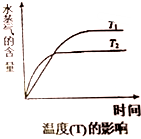
(4)在恒压密闭容器中,由CO2和H2进行反应I合成甲醇,在其它条件不变的情况下,探究温度对化学平衡的影响,实验结果如图.
①△H1<0(填“>”、“<”或“=”)
②有利于提高CO2平衡转化率的措施有A(填标号).
A.降低反应温度
B.投料比不变,增加反应物的浓度
C.增大CO2和H2的初始投料比
D.混合气体中掺入一定量惰性气体(不参与反应)
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为P0,仅进行反应I.
①充分反应达到平衡后,若CO2转化率为a,则容器的压强与起始压强之比为$\frac{2-a}{2}$(用a表示).
②若经过3h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为0.5mol•L-1•h-1(保留三位有效数字);该温度下反应的化学平衡常数K为0.148(L•mol-1)2(保留三位有效数字);平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数.写出上述反应压力平衡常数KP为$\frac{64}{27{P}_{0}^{2}}$(用P0表示,并化简).
0 157411 157419 157425 157429 157435 157437 157441 157447 157449 157455 157461 157465 157467 157471 157477 157479 157485 157489 157491 157495 157497 157501 157503 157505 157506 157507 157509 157510 157511 157513 157515 157519 157521 157525 157527 157531 157537 157539 157545 157549 157551 157555 157561 157567 157569 157575 157579 157581 157587 157591 157597 157605 203614
 研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ
CO2(g)+H2(g)?CO(g)+H2O(g)△H2=+41.2kJ•mol-8平衡常数K2 反应Ⅱ
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如表实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
(1)合成的甲醇可用于燃料电池的燃料,若电解质为稀烧碱溶液时甲醇燃料电池的正极反应式为O2+4e-+2H2O=4OH-;研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在阴极,该电极反应式是CO2+6e-+6H+=CH3OH+H2O.
(2)从表中实验数据可以分析出,提高CO2转化成CH3OH的选择性的方法有使用Cat2催化剂(或理想催化剂);温度为543K(或降低温度).
(3)反应CO(g)+2H2(g)?CH3OH(g)的平衡常数K3=$\frac{{K}_{1}}{{K}_{2}}$(用K1和K2表示).
(4)在恒压密闭容器中,由CO2和H2进行反应I合成甲醇,在其它条件不变的情况下,探究温度对化学平衡的影响,实验结果如图.
①△H1<0(填“>”、“<”或“=”)
②有利于提高CO2平衡转化率的措施有A(填标号).
A.降低反应温度
B.投料比不变,增加反应物的浓度
C.增大CO2和H2的初始投料比
D.混合气体中掺入一定量惰性气体(不参与反应)
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为P0,仅进行反应I.
①充分反应达到平衡后,若CO2转化率为a,则容器的压强与起始压强之比为$\frac{2-a}{2}$(用a表示).
②若经过3h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为0.5mol•L-1•h-1(保留三位有效数字);该温度下反应的化学平衡常数K为0.148(L•mol-1)2(保留三位有效数字);平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数.写出上述反应压力平衡常数KP为$\frac{64}{27{P}_{0}^{2}}$(用P0表示,并化简).
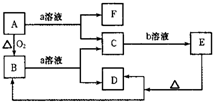 已知如图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体.且各种物质所含元素除H、O外,其余均为第三周期元素.
已知如图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体.且各种物质所含元素除H、O外,其余均为第三周期元素.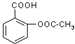 试根据阿斯匹林的结构回答;
试根据阿斯匹林的结构回答; ,其分子式为C7H6O3,则B的结构简式为CH3COOH;
,其分子式为C7H6O3,则B的结构简式为CH3COOH;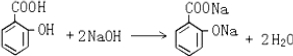 .
.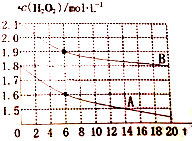 现有如下溶液:①1.0mL0.10mol•L-1双氧水 ②1.0mL0.20mol•L-1双氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢:
现有如下溶液:①1.0mL0.10mol•L-1双氧水 ②1.0mL0.20mol•L-1双氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢: