9.某同学学习了化学反应速率后,联想到曾用H2O2制备氧气,于是设计了下面的实验方案并进行实验探究.
【查阅资料】过氧化氢(H2O2),其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定.在加热的条件下,它能分解生成氧气.研究表明,将新制的5%的H2O2溶液加热到65℃时就有氧气放出,加热到80℃时就有较多氧气产生.
(1)上述实验发生反应的化学方程式为2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑.
(2)实验甲和实验乙的实验目的是探究反应物的不同浓度对反应速率的影响;实验丙、实验丁和实验戊的实验目的是探究在不同酸碱性条件下,催化剂对反应速率的影响.
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的?
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如表.
①对实验戊,0~20s的反应速率v1=0.775mL/s,100~120s的反应速率v2=0.575mL/s.不考虑实验测量误差,二者速率存在差异的主要原因是随反应的不断进行,H2O2溶液的浓度逐渐降低,反应速率减小.
②如图是根据实验收集到最大体积的气体时所用时间绘制的图象.曲线c表示的是实验丁(填“丙”、“丁”或“戊”).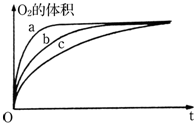
| 实验编号 | 反应物 | 催化剂 |
| 甲 | 试管中加入3mL 2%H2O2溶液和3滴蒸馏水 | 无 |
| 乙 | 试管中加入3mL 5%H2O2溶液和3滴蒸馏水 | 无 |
| 丙 | 试管中加入3mL 5%H2O2溶液和3滴蒸馏水 | 1mL 0.1mol/L FeCl3溶液 |
| 丁 | 试管中加入3mL 5%H2O2溶液和3滴稀盐酸溶液 | 1mL 0.1mol/L FeCl3溶液 |
| 戊 | 试管中加入3mL 5%H2O2溶液和3滴NaOH溶液 | 1mL 0.1mol/L FeCl3溶液 |
(1)上述实验发生反应的化学方程式为2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑.
(2)实验甲和实验乙的实验目的是探究反应物的不同浓度对反应速率的影响;实验丙、实验丁和实验戊的实验目的是探究在不同酸碱性条件下,催化剂对反应速率的影响.
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的?
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如表.
| 时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
| 气体体积/mL | 实验丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
| 实验丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
| 实验戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
②如图是根据实验收集到最大体积的气体时所用时间绘制的图象.曲线c表示的是实验丁(填“丙”、“丁”或“戊”).

8.下列金属防腐的措施中,属于牺牲阳极的阴极保护法的是( )
| A. | 水中的钢闸门连接电源的负极 | |
| B. | 地下钢管连接锌板 | |
| C. | 铁件镀铜 | |
| D. | 自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 |
7.科学家预言,燃料电池将是 21 世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极催化剂,工作原理是将电极插入KOH溶液中,然后在两极分别添加甲醇和氧气,若a极上添加甲醇;b极:2H2O+O2+4e-═4OH-. 关于此燃料电池的下列说法中错误的是( )
| A. | a极为负极,b极为正极 | |
| B. | 放电过程中,a、b电极上均发生氧化还原反应 | |
| C. | 该电池工作时添加甲醇的一极,附近溶液的碱性减弱,反应的离子方程式为:CH3OH+8OH--6e-═CO32-+6H2O | |
| D. | 若用此电源电解饱和食盐水,每消耗0.1molO2则阳极理论上生成0.2molCl2 |
6.除去下列括号内杂质的试剂或方法错误的是( )
| A. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | FeCl2溶液(FeCl3),铁粉,过滤 | |
| D. | CO(CO2),氢氧化钠溶液,洗气 |
5.下列反应中水作还原剂的是( )
| A. | F2+H2O | B. | Cl2+H2O | C. | Na+H2O | D. | Na2O2+H2O |
4.将1mol 乙酸(其羟基氧用 18O 标记)与乙醇在浓硫酸并加热条件下发生反应(不考虑副反应).下列叙述正确的是( )
| A. | 浓硫酸只起到吸水作用,不参与反应 | |
| B. | 反应体系中含18O的分子有2种 | |
| C. | 乙酸乙酯中还有18O 原子 | |
| D. | 反应一段时间后乙醇中含有18O原子 |
3.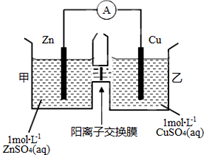 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )| A. | Zn电极上发生氧化反应 | |
| B. | 电子的流向为Zn→电流表→Cu | |
| C. | SO42-由乙池通过离子交换膜向甲池移动 | |
| D. | 电池工作一段时间后,乙池溶液的总质量明显增加 |
2.下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是( )
0 157393 157401 157407 157411 157417 157419 157423 157429 157431 157437 157443 157447 157449 157453 157459 157461 157467 157471 157473 157477 157479 157483 157485 157487 157488 157489 157491 157492 157493 157495 157497 157501 157503 157507 157509 157513 157519 157521 157527 157531 157533 157537 157543 157549 157551 157557 157561 157563 157569 157573 157579 157587 203614
| A. | 三种微粒所含有的电子数相等 | B. | 三种微粒中氮原子的杂化方式相同 | ||
| C. | 三种微粒的空间构型相同 | D. | 键角大小关系:NH4+>NH3>NH2- |