20.某地环保部门取一定量某工厂所排废水试样分成甲、乙、丙、丁四份,进行如图所示探究.
已知废水试样中可能含有下表中的离子:
(1)离子X是NH4+(填化学式,下同),离子Y是SO42-.
(2)表中不能确定是否存在的阴离子是Cl-,能证明该阴离子是否存在的简单实验操作为取少量废水试样,滴加足量的Ba(NO3)2溶液,静置,取上层清液,滴加硝酸酸化的AgNO3溶液,若有白色沉淀产生,则存在Cl-,若无白色沉淀产生,则不存在.
(3)丁组实验在酸性条件下发生反应的离子方程式是6I-+2NO3-+8H+=2NO↑+3I2+4H2O.

已知废水试样中可能含有下表中的离子:
| 阳离子 | Na+、Mg2+、X |
| 阴离子 | Cl-、SO32-、Y、NO3- |
(2)表中不能确定是否存在的阴离子是Cl-,能证明该阴离子是否存在的简单实验操作为取少量废水试样,滴加足量的Ba(NO3)2溶液,静置,取上层清液,滴加硝酸酸化的AgNO3溶液,若有白色沉淀产生,则存在Cl-,若无白色沉淀产生,则不存在.
(3)丁组实验在酸性条件下发生反应的离子方程式是6I-+2NO3-+8H+=2NO↑+3I2+4H2O.
18.把一定质量的铁完全溶解于某浓度的硝酸中收集到0.3mol NO2和0.2mol NO.向反应后的溶液中加入足量NaOH溶液充分反应,经过滤、洗涤后,把所得沉淀加热至质量不再减少为止.得到固体质量不可能为( )
| A. | 18 g | B. | 24 g | C. | 30 g | D. | 36 g |
17.下列离子方程式书写正确的是( )
| A. | 在100 mL浓度为1 mol•L-1的 Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | 在100 mL浓度为2 mol•L-1的FeI2的溶液中通入标准状况下5.6 L的Cl2:4Fe2++6I-+5Cl2═4Fe3++3I2+10Cl- | |
| C. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
16.下列有关说法正确的是( )
| A. | 丙烯的结构简式为CH2CHCH3 | |
| B. | 新戊烷的二氯代物有2种 | |
| C. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| D. | 键线式为 的有机物的分子式为C8H10 的有机物的分子式为C8H10 |
15.下列叙述中不正确的是( )
| A. | 用石墨作电极电解CuSO4溶液,通电一段时间后,在标准状况下两极产生的气体可能相等 | |
| B. | 船底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-═4OH- | |
| D. | 电解池中的阳极和原电池中的负极上都发生还原反应 |
14.在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如表.下列判断正确的是( )
0 157390 157398 157404 157408 157414 157416 157420 157426 157428 157434 157440 157444 157446 157450 157456 157458 157464 157468 157470 157474 157476 157480 157482 157484 157485 157486 157488 157489 157490 157492 157494 157498 157500 157504 157506 157510 157516 157518 157524 157528 157530 157534 157540 157546 157548 157554 157558 157560 157566 157570 157576 157584 203614
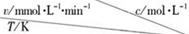 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a=7.50 | |
| B. | 同时改变反应温度和蔗糖的浓度,v可能不变 | |
| C. | b>318.2 | |
| D. | 温度为b时,蔗糖浓度减少一半所需的时间比318.2K时短 |
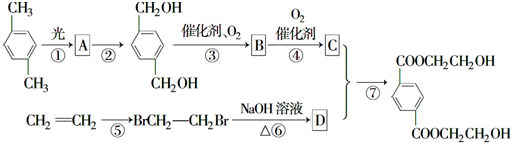
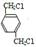 ,B
,B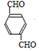 ,
,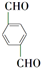 +O2$\stackrel{催化剂}{→}$
+O2$\stackrel{催化剂}{→}$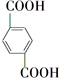
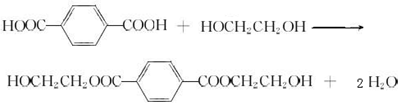
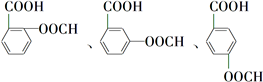 .
.