1.将1mol两种气态烃组成的混合气体完全燃烧后,将得到产物依次通入浓硫酸和石灰水中,其中浓硫酸质量增加了36g,并生成了150g沉淀.下列说法正确的是( )
| A. | 一定有乙烷 | B. | 一定有甲烷 | C. | 一定没有甲烷 | D. | 不一定有甲烷 |
18.下列装置,可达到铁片上镀锌目的是( )
| A. |  含Fe2+电镀液 | B. | 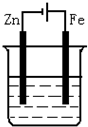 含Fe2+电镀液 | C. |  含Zn2+电镀液 | D. | 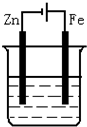 含Zn2+电镀液 |
15.对于平衡体系2SO2(g)+O2(g)?2SO3(g)△H<0.下列结论中正确的是( )
| A. | 若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.5倍 | |
| B. | 若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量这比为2:1 | |
| C. | 若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率 | |
| D. | 平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2 |
14.关于如图原电池装置的说法正确的是( )

| A. | Cu一定为正极 | |
| B. | 若溶液中的阴离子移向铁电极,则电流由铜电极经导线流向铁电极 | |
| C. | 若铜电极增重,则X可能为CuSO4、AgNO3、FeCl3等 | |
| D. | 若铜电极溶解,则铁电极表面可能有无色刺激性气味的气体产生 |
13.下列关于热化学反应反应的描述中正确的是( )
| A. | 已知H+(aq)+OH-(aq)═H20(l)△H=-57.3kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=-2×(-57.3)kJ•mol-1 | |
| B. | 由4P(s,红磷)═P4(s,白磷)△H=+139.2kJ/mol可知,红磷比白磷稳定 | |
| C. | H2(g)的燃烧热是285.8kJ•mol-1,则2H2O═2H2(g)+O2(g)△H=+571.6KJ•mol-1 | |
| D. | 恒温恒容时,将2molA和1molB投入密闭容器中,发生反应:2A(g)+B(g)?2C(g).充分反应后测得放出的热量为QkJ,则该反应的△H=-QkJ/mol |
12.下列关于电池的说法正确的是( )
0 157380 157388 157394 157398 157404 157406 157410 157416 157418 157424 157430 157434 157436 157440 157446 157448 157454 157458 157460 157464 157466 157470 157472 157474 157475 157476 157478 157479 157480 157482 157484 157488 157490 157494 157496 157500 157506 157508 157514 157518 157520 157524 157530 157536 157538 157544 157548 157550 157556 157560 157566 157574 203614
| A. | 电解含CuSO4和NaCl的溶液,在阴极可能析出气体,阳极一定析出气体 | |
| B. | 电解CuCl2溶液可得到铜和氯气,阴极区酸性减弱,阳极区pH不变 | |
| C. | 碱性锌锰干电池的负极反应为:Zn-2e-+4OH-═ZnO22-+2H2O | |
| D. | 原电池负极金属一定比正极金属的金属性活泼 |

 利用LiOH和钴氧化物可制备锂离子电池正极材料.LiOH可由电解法制备,利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.B极区电解液为LiOH溶液(填化学式),阳极电极反应式为2Cl--2e-=Cl2↑,电解过程中Li+向B电极迁移(填“A”或“B”).
利用LiOH和钴氧化物可制备锂离子电池正极材料.LiOH可由电解法制备,利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.B极区电解液为LiOH溶液(填化学式),阳极电极反应式为2Cl--2e-=Cl2↑,电解过程中Li+向B电极迁移(填“A”或“B”).