18.一定温度下,在2.0L的密闭容器中充入0.1molN2O和0.1molCO,在一定条件下发生催化反应:N2O(g)+CO(g)?催化剂N2(g)+CO2(g).依据下列图象作出的判断正确的是( )
| A. |  由图可判断该反应的正反应为放热反应 | |
| B. |  由图可判断阴影部分面积的数值为0.05 | |
| C. |  由图可判断横坐标X可能是压强 | |
| D. |  图研究的是不同催化剂对反应的影响,则甲使用的催化剂效率较高 |
17.4-溴甲基-1-环已烯的一种合成路线如下:

下列说法正确的是( )

下列说法正确的是( )
| A. | 化合物X、Y、Z中均有一个手性碳原子 | |
| B. | ①、②、③的反应类型依次为加成反应、还原反应和取代反应 | |
| C. | 由化合物Z一步制备化合物Y的转化条件是:NaOH醇溶液,加热 | |
| D. | 化合物Y先经酸性高锰酸钾溶液氧化,再与乙醇在浓硫酸催化下酯化可制得化合物X |
16.NH3-O2碱性燃料电池的示意图如下,有关说法正确的是( )

| A. | 该电池总反应为:4NH3+3O2═2N2+6H2O | |
| B. | a极的电极反应为:2NH3-6e-═N2+6H+ | |
| C. | b极的电极反应为:4OH--4e-═2H2O+O2↑ | |
| D. | a极每产生1molN2,约有6×6.02×1023个OH-迁移至b极 |
15.25℃时,下列有关曲线与对应的叙述正确的是( )
| A. | 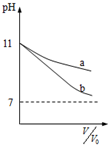 图可表示体积均为V0L、pH均为11的氨水与NaOH溶液分别用水稀释至VL情况,则b曲线为氨水 | |
| B. | 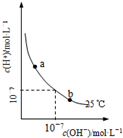 图可表示水溶液中H+与OH-的浓度变化曲线,则升高温度可实现a→b | |
| C. | 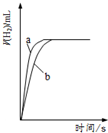 图可表示体积均为100mL、pH均为3的盐酸与醋酸,分别与0.003gZn反应,则a表示盐酸 | |
| D. | 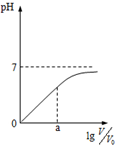 图可表示体积为V0L1 mol•L-1盐酸用水稀释至VL情况,则0~a范围内:pH=lg$\frac{V}{{V}_{0}}$ |
14.下列可逆反应平衡常数,其表达式或与有关常数的关系正确的是( )
| A. | 反应C(s)+H2O(g)?CO(g)+H2(g) 的平衡常数为:K=$\frac{c(CO)•c({H}_{2})}{c(C)•c({H}_{2}O)}$ | |
| B. | 反应Cr2O72-+H2O?2CrO42-+2H+ 的平衡常数为:K=$\frac{c(Cr{O}_{4}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{O}_{3}^{2-})•c({H}_{2}O)}$ | |
| C. | NH4++H2O?NH3•H2O+H+的平衡常数为:K=$\frac{{K}_{W}}{{K}_{b}(N{H}_{3}•{H}_{2}O)}$ | |
| D. | 2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq)的平衡常数为:K=$\frac{{K}_{sp}(A{g}_{2}S)}{{{K}_{sp}}^{2}(AgI)}$ |
13.下列滴定反应不需要用指示剂的是( )
0 157351 157359 157365 157369 157375 157377 157381 157387 157389 157395 157401 157405 157407 157411 157417 157419 157425 157429 157431 157435 157437 157441 157443 157445 157446 157447 157449 157450 157451 157453 157455 157459 157461 157465 157467 157471 157477 157479 157485 157489 157491 157495 157501 157507 157509 157515 157519 157521 157527 157531 157537 157545 203614
| A. | 硝酸银标准溶液滴定含氯离子的溶液[Ag++Cl-═AgCl↓] | |
| B. | 盐酸标准溶液滴定氨水[H++NH3•H2O═NH4++H2O] | |
| C. | Na2S2O3标准溶液滴定含单质碘的溶液[I2+2Na2S2O3(无色)═Na2S4O6 (无色)+2NaI] | |
| D. | 酸性高锰酸钾标准溶液滴定草酸溶液[2MnO4-+5H2C2O4+6H+═2Mn2+(无色)+10CO2↑+8H2O] |



 的路线如下:
的路线如下:
 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.