19.下列物质中既含有离子键又含有共价键的是( )
| A. | HCl | B. | KOH | C. | I2 | D. | Na2 O |
18.碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛.完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜.写出该反应的化学方程式4KI+2CuSO4=I2+Cu2I2↓+2K2SO4.
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去.写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是H2SO3、KI、Cu2I2.
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2+Hg═Cu2HgI4(玫瑰红)+2Cu,产物Cu2HgI4中Cu元素显+1价.当有1molCu2I2参与反应时,转移电子1mol.
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作.试剂M和操作N的组合正确的是bd(选填编号)
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜.写出该反应的化学方程式4KI+2CuSO4=I2+Cu2I2↓+2K2SO4.
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去.写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是H2SO3、KI、Cu2I2.
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2+Hg═Cu2HgI4(玫瑰红)+2Cu,产物Cu2HgI4中Cu元素显+1价.当有1molCu2I2参与反应时,转移电子1mol.
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作.试剂M和操作N的组合正确的是bd(选填编号)
| 选项 | 试剂M | 操作N |
| a | 碘化钾溶液 | 升华 |
| b | 氢碘酸溶液 | 萃取分液 |
| c | 氢气 | 过滤 |
| d | 氢硫酸溶液 | 过滤 |
17.在下列水溶液中进行的反应,在反应过程中既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键生成的是( )
| A. | 2NaBr+Cl2═2NaCl+Br2 | B. | 2Na+H2O═2NaOH+H2 | ||
| C. | 2Na2O2+2H2O═2NaOH+O2 | D. | Na+Cl2═2NaCl |
16.下列反应的离子方程式不正确的是( )
| A. | Cl2与稀NaOH溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | Fe2(SO4)3和KI溶液反应:Fe3++2I-═Fe2++I2 | |
| C. | 烧碱溶液中加入铝片:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O |
15.下列离子能在溶液中大量共存的是( )
| A. | Na+、NH4+、CO32-、Br- | B. | Fe2+、H+、NO3-、Cl- | ||
| C. | Al3+、Ca2+、HCO3-、SO42- | D. | Fe3+、Cu2+、NO3-、OH- |
12.下列金属晶体中,自由电子与金属阳离子间的作用力最弱的是( )
0 157347 157355 157361 157365 157371 157373 157377 157383 157385 157391 157397 157401 157403 157407 157413 157415 157421 157425 157427 157431 157433 157437 157439 157441 157442 157443 157445 157446 157447 157449 157451 157455 157457 157461 157463 157467 157473 157475 157481 157485 157487 157491 157497 157503 157505 157511 157515 157517 157523 157527 157533 157541 203614
| A. | Na | B. | K | C. | Mg | D. | Al |
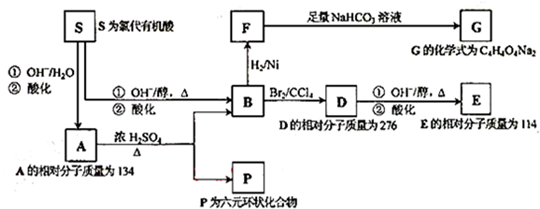
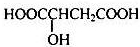 、P:
、P: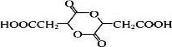 、E:HOOCC≡CCOOH、S:
、E:HOOCC≡CCOOH、S: .
. .
.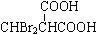
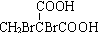 .
.
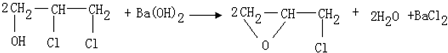 ;
;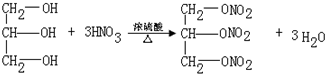 .
.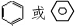 .乙烯与溴水的反应是加成反应.把甲烷和氯气混合在一起的试管倒置在装有饱和食盐水的水槽中进行光照有几种产物5种,最多的是氯化氢.
.乙烯与溴水的反应是加成反应.把甲烷和氯气混合在一起的试管倒置在装有饱和食盐水的水槽中进行光照有几种产物5种,最多的是氯化氢.