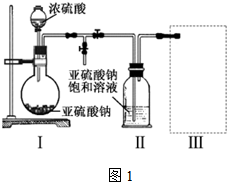
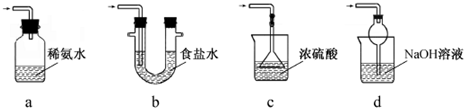
12.有一固体混合物,可能含有阴离子:NO${\;}_{3}^{-}$、SO42-、SO32-、CO32-、AlO${\;}_{2}^{-}$,阳离子:K+、Al3+、Cu2+、NH${\;}_{4}^{+}$、Na+.为了鉴定其中的离子,现进行如下实验,实验现象和结论相符的是( )
| A. | 向溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,说明一定含有SO${\;}_{4}^{2-}$ | |
| B. | 向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有气体逸出,说明一定存在CO32-和AlO${\;}_{2}^{-}$ | |
| C. | 用焰色反应检验时,透过蓝色钴玻璃观察火焰呈紫色,则说明含有K+没有Na+ | |
| D. | 取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12,说明不存在NH${\;}_{4}^{+}$、Al3+、Cu2+ |
10.某溶液可能含有Cl-、SO42-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH 溶液,加热,得到0.02mol 气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g 固体;向上述滤液中加足量BaCl2溶液,得到 4.66g 不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在5 种离子 | |
| B. | SO42-、NH4+、Fe3+、一定存在,Cl-、K+、Al3+可能存在 | |
| C. | K+一定存在,Al3+可能存在 | |
| D. | Cl-一定存在,且c(Cl-)≥0.4mol/L |
9.J、L、R、T是原子序数依次增大的短周期主族元素,其中J、R、T在周期表中的相对位置如右表:J元素最外层电子数是电子层数的2倍.L与R同周期,且L在该周期中原子半径最大.
(1)R 2-的离子结构示意图为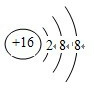 .
.
(2)写出L元素与T元索组成化合物的电子式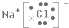 .
.
(3)写出实验室制备单质T2的离子反应方程式MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(4)单质T2与石灰乳反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(5)单质L与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
(6)由J、R形成的液态化合物JR20.2mol在O2中完全燃烧,生成两种气态氧化物,放出热量215kJ.则该反应的热化学方程式为CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075kJ•mol-1.
| J | ||||
| R | T |
 .
.(2)写出L元素与T元索组成化合物的电子式
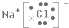 .
.(3)写出实验室制备单质T2的离子反应方程式MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(4)单质T2与石灰乳反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(5)单质L与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
(6)由J、R形成的液态化合物JR20.2mol在O2中完全燃烧,生成两种气态氧化物,放出热量215kJ.则该反应的热化学方程式为CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075kJ•mol-1.
8.下列有关结构和性质的说法中,正确的是( )


| A. | 主族元素原子的最外层电子数越多,元素的金属性越强 | |
| B. | C、N、0、F元素的单质与氢气化合越来越剧烈 | |
| C. | 图是元素周期表中碘元素的部分信息,可知该碘原子的质量数为126.9 | |
| D. | 元素在周期表中的族序数与该元素原子电子层数相等 |
7.用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4•H2O的工艺流程如下:
Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度.
(1)步骤Ⅰ中,滤渣的主要成分是二氧化硅.
(2)将MnO2氧化Fe2+的离子方程式补充完整:
□MnO 2+□Fe 2++□═Mn 2++□Fe 3++□□
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、不会引入Cl-,使制得的MnSO4?H2O产品更纯净.
(4)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol/L
步骤Ⅲ中a的取值范围是4.7≤a<7.6.
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度.
已知一定条件下,MnO4-与Mn2+反应生成MnO2.取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为$\frac{1.5y×1{0}^{-4}×55}{x}$.
Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度.
(1)步骤Ⅰ中,滤渣的主要成分是二氧化硅.
(2)将MnO2氧化Fe2+的离子方程式补充完整:
□MnO 2+□Fe 2++□═Mn 2++□Fe 3++□□
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、不会引入Cl-,使制得的MnSO4?H2O产品更纯净.
(4)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
步骤Ⅲ中a的取值范围是4.7≤a<7.6.
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度.
已知一定条件下,MnO4-与Mn2+反应生成MnO2.取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为$\frac{1.5y×1{0}^{-4}×55}{x}$.
3.某有机物在O2中充分燃烧,生成CO2和H2O的物质的量比为1:1,下列说法正确的是( )
0 157317 157325 157331 157335 157341 157343 157347 157353 157355 157361 157367 157371 157373 157377 157383 157385 157391 157395 157397 157401 157403 157407 157409 157411 157412 157413 157415 157416 157417 157419 157421 157425 157427 157431 157433 157437 157443 157445 157451 157455 157457 157461 157467 157473 157475 157481 157485 157487 157493 157497 157503 157511 203614
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:1 | ||
| C. | 该有机物可能为烃 | D. | 此有机物的最简式为CH2 |
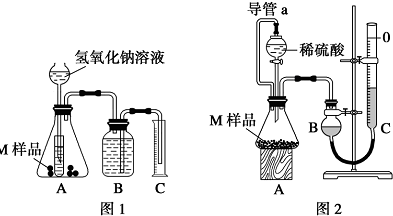
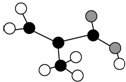 (1)经分析,某芳香族化合物A含C、H、O的质量分数分别为77.8%、7.4%、14.8%,该有机物一个分子中只含有一个氧原子.
(1)经分析,某芳香族化合物A含C、H、O的质量分数分别为77.8%、7.4%、14.8%,该有机物一个分子中只含有一个氧原子.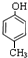 ;
; 一名同学把4.48L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
一名同学把4.48L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8mol Ca(OH)2的澄清石灰水的烧杯,如图所示: .
.