2.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行滴定操作:
选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是③.(填序号)除以上仪器外还缺的玻璃仪器有250mL容量瓶中、胶头滴管.
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
请完成下列问题:
(1)正确的操作步骤是(填写字母)C→A→B→D→E.
(2)滴定管读数应注意滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到0.01ml.
(3)操作中锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(4)操作D中液面应调整到调节到零刻度或零稍下的某一刻度,充满标准H2SO4溶液;
(5)滴定到终点时锥形瓶内溶液的pH约为4;终点时的颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响偏高(填“偏高”、“偏低”或“无影响”,其他操作均正确).
选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是③.(填序号)除以上仪器外还缺的玻璃仪器有250mL容量瓶中、胶头滴管.
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
| 指示剂 | 变色范围 | 酸色 | 碱色 |
| 石蕊 | 5.0-8.0 | 红色 | 蓝色 |
| 酚酞 | 8.0-10.0 | 无色 | 红色 |
| 甲基橙 | 3.1-4.4 | 红色 | 黄色 |
(1)正确的操作步骤是(填写字母)C→A→B→D→E.
(2)滴定管读数应注意滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到0.01ml.
(3)操作中锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(4)操作D中液面应调整到调节到零刻度或零稍下的某一刻度,充满标准H2SO4溶液;
(5)滴定到终点时锥形瓶内溶液的pH约为4;终点时的颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响偏高(填“偏高”、“偏低”或“无影响”,其他操作均正确).
20.下列电子式书写正确的是( )
| A. | 氮气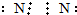 | B. | 氨基H:N:H | ||
| C. | 过氧化氢H+[:O:]2-H+ | D. | 氯化钠Na+[:Cl:]- |
19.实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是( )
| A. | 加水稀释 | B. | 加少量NaOH溶液 | C. | 改用98%的浓硫酸 | D. | 锌片改为锌粒 |
18.下列有关化学用语表示正确的是( )
| A. | H2O2的电子式: | |
| B. | 铝离子的结构示意图: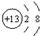 | |
| C. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{45}$Br | |
| D. | ${\;}_{6}^{14}$C与${\;}_{6}^{12}$C互为同素异形体 |
17.化学与生活、社会密切相关.“低碳经济,节能减排”是今后经济发展的新思路.下列说法不正确的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 将废弃的秸秆转化为清洁高效的能源 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 采用新技术开采煤、石油和天然气,以满足经济发展的需要 |
14.下列说法不正确的是( )
0 157306 157314 157320 157324 157330 157332 157336 157342 157344 157350 157356 157360 157362 157366 157372 157374 157380 157384 157386 157390 157392 157396 157398 157400 157401 157402 157404 157405 157406 157408 157410 157414 157416 157420 157422 157426 157432 157434 157440 157444 157446 157450 157456 157462 157464 157470 157474 157476 157482 157486 157492 157500 203614
| A. | 已知冰的熔化热为6.0 kJ•mol-1,冰中氢键键能为20 kJ•mol-1,假设1 mol 冰中有2 mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,电离常数K$\frac{(ca)^{2}}{c(1-a)}$=.若加水稀释,则CH3COOH?CH3C00-+H+向右移动,a增大,Ka不变 | |
| C. | 甲烷的标准燃烧热为-890.3 kjJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH3 (g)+202(g)-C02(g)+2H20(1)△H=-890.3 kJ•mol-1 | |
| D. | 500℃、30 MPa下,将0.5 mol N和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)$?_{500℃,30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 |
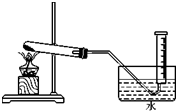 为验证MnO2在KClO3受热分解制02的反应前后质量不变,某兴趣小组利用如图所示装置进行了如下实验:
为验证MnO2在KClO3受热分解制02的反应前后质量不变,某兴趣小组利用如图所示装置进行了如下实验: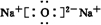 、
、 .
.