20.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,22.4L O2所含的原子数为2NA | |
| B. | 标准状况下,22.4L H2所含的分子数为NA | |
| C. | 标准状况下,22.4L H2O所含的分子数为NA | |
| D. | 56g铁粉与盐酸完全反应时转移电子数为3NA |
19.下列物质中不属于高分子化合物的是( )
| A. | 蛋白质 | B. | 硝酸甘油脂 | C. | 硝酸纤维素脂 | D. | 天然橡胶 |
18.质量比为2:1的H2SO4和H3PO4,它们所含氢原子物质的量之比是( )
| A. | 2:1 | B. | 2:3 | C. | 4:3 | D. | 1:1 |
17.在恒容的密闭容器中发生反应H2(g)+I2(g)?2HI(g),下列可以说明反应达到平衡状态的是( )
①单位时间内生成n mol I2的同时生成2n mol HI
②单位时间内生成n mol H2的同时生成2n mol I2
③混合气体的颜色不再改变
④混合气体的物质的量不再改变.
①单位时间内生成n mol I2的同时生成2n mol HI
②单位时间内生成n mol H2的同时生成2n mol I2
③混合气体的颜色不再改变
④混合气体的物质的量不再改变.
| A. | ①③ | B. | ②④ | C. | ①③④ | D. | ①②③④ |
15.下列说法正确的是( )
| A. | 天然橡胶分子中含有碳碳双键,能发生加成反应 | |
| B. | 硫化橡胶遇汽油能发生溶胀现象 | |
| C. | 聚硫橡胶具有良好的耐严寒,耐高温性能 | |
| D. | 合成橡胶是以石油、天然气为原料,以二烯烃和烯烃为单体聚合而成分高分子 |
14.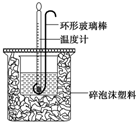 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
(1)碎泡沫塑料的作用是保温隔热,减少热量损失环形玻璃搅拌棒可不可以用铜丝搅拌棒代替,为什么不可以;铜的导热性好,易损失热量产生误差
(2)该实验测得的中和热数值为56.8 kJ•mol-1,(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算).
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值偏小(“偏大”、“偏小”或“不变”)
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃[来源:Z,xx,k.Com] | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.3 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 20.5 | 20.6 | 24.9 |
(2)该实验测得的中和热数值为56.8 kJ•mol-1,(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算).
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值偏小(“偏大”、“偏小”或“不变”)
13.为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论正确的是( )
0 157301 157309 157315 157319 157325 157327 157331 157337 157339 157345 157351 157355 157357 157361 157367 157369 157375 157379 157381 157385 157387 157391 157393 157395 157396 157397 157399 157400 157401 157403 157405 157409 157411 157415 157417 157421 157427 157429 157435 157439 157441 157445 157451 157457 157459 157465 157469 157471 157477 157481 157487 157495 203614
| A. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,可看到有氢气生成 | |
| B. | 将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度NaOH溶液反应,前者速率大于后者 | |
| C. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 | |
| D. | 大理石和盐酸反应制取CO2,增加大理石的用量可加快反应速率 |
