11.10℃加热NaHCO3饱和溶液,测得该溶液的pH发生如下的变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该水解反应的离子方程式为HCO3-+H2O?H2CO3+OH-.
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3,该分解反应的方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(3)丙同学认为甲、乙的判断都不充分.丙认为:
①只要在加热煮沸的溶液中加入足量的试剂BaCl2溶液,若产生沉淀,则乙判断正确.原因是加入氯化钡溶液后,如生成沉淀,说明溶液中存在大量的CO32-,Ba2++CO32-=BaCO3↓.
能不能选用Ba(OH)2溶液?不能(答“能”或“不能”)
②将加热后的溶液冷却到10℃,若溶液的pH等于(填“大于”、“小于”或“等于”)8.3,则甲(填“甲”或“乙”)判断正确.
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| PH | 8.3 | 8.4 | 8.5 | 8.8 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3,该分解反应的方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(3)丙同学认为甲、乙的判断都不充分.丙认为:
①只要在加热煮沸的溶液中加入足量的试剂BaCl2溶液,若产生沉淀,则乙判断正确.原因是加入氯化钡溶液后,如生成沉淀,说明溶液中存在大量的CO32-,Ba2++CO32-=BaCO3↓.
能不能选用Ba(OH)2溶液?不能(答“能”或“不能”)
②将加热后的溶液冷却到10℃,若溶液的pH等于(填“大于”、“小于”或“等于”)8.3,则甲(填“甲”或“乙”)判断正确.
8.下列关于盐类水解的说法错误的是( )
| A. | pH相等的①NaHCO3、②Na2CO3、③NaOH溶液的物质的量浓度大小:③>②>① | |
| B. | 浓度均为0.1mol/L的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为:①>②>③ | |
| C. | 在NH4Cl溶液中加入稀HNO3,能抑制NH4+水解 | |
| D. | 在CH3COONa溶液中加入冰醋酸,能控制CH3COO-水解 |
7.下列各组离子在指定溶液中,一定能大量共存的是( )
| A. | 在由水电离出的c(OH-)=1×10-13mol/L的溶液中:Na+、Al3+、Cl-、NO3- | |
| B. | 在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| C. | 在澄清透明的溶液中:Cu2+、K+、SO42-、Cl- | |
| D. | 在能使甲基橙变黄色的溶液中:Na+、CO32-、NO3-、K+ |
6.下列各式中,属于正确的电离方程式的是( )
| A. | HCO3-+H2O?H2CO3+OH- | B. | HS-+H2O?S2-+H3O- | ||
| C. | HCO3-+H2O?H3O++CO32- | D. | H3PO4?3H++PO43+ |
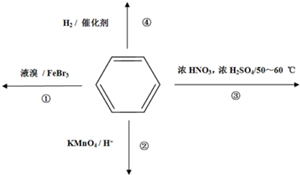
3.下列关于苯的叙述正确的是( )
0 157296 157304 157310 157314 157320 157322 157326 157332 157334 157340 157346 157350 157352 157356 157362 157364 157370 157374 157376 157380 157382 157386 157388 157390 157391 157392 157394 157395 157396 157398 157400 157404 157406 157410 157412 157416 157422 157424 157430 157434 157436 157440 157446 157452 157454 157460 157464 157466 157472 157476 157482 157490 203614

| A. | 反应①为取代反应,有机产物与水混合浮在上层 | |
| B. | 反应②为氧化反应,反应现象是火焰为淡蓝色 | |
| C. | 反应③为取代反应,有机产物是一种烃的衍生物 | |
| D. | 反应④中1 mol苯最多与6 mol H2发生加成反应 |

