2. (1)已知:①C(s)+O2(g)=CO2(g)△H=a kJ•mol-1
(1)已知:①C(s)+O2(g)=CO2(g)△H=a kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=b kJ•mol-1;
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=c kJ•mol-1;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=c+2a-bkJ•mol-1.(用含a、b、c的式子表示)
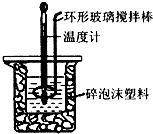
(2)用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
①该实验中,量取50mL盐酸或NaOH溶液,需要用到的玻璃仪器除胶头滴管外还要50ml量筒;
②装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失;
③某同学实验记录的数据如上表所示,其中记录的终止温度是指混合溶液的最高温度;
④计算该实验发生中和反应时放出的热量为1344J[中和后生成的溶液的比热容c=4.2J•(g•℃)-1,稀溶液的密度都为1g•cm-3];
⑤若用50mL 0.55mol•L-1的氨水(NH3•H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H会偏大(填“偏大”、“偏大”或“不变”,其原因是一水合氨为弱电解质,反应过程中电离需要吸收热量,故放出的热量偏少,△H偏大.
 (1)已知:①C(s)+O2(g)=CO2(g)△H=a kJ•mol-1
(1)已知:①C(s)+O2(g)=CO2(g)△H=a kJ•mol-1②2CO(g)+O2(g)=2CO2(g)△H=b kJ•mol-1;
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=c kJ•mol-1;
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=c+2a-bkJ•mol-1.(用含a、b、c的式子表示)
(2)用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | |||
| 平均值 | |||||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
②装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失;
③某同学实验记录的数据如上表所示,其中记录的终止温度是指混合溶液的最高温度;
④计算该实验发生中和反应时放出的热量为1344J[中和后生成的溶液的比热容c=4.2J•(g•℃)-1,稀溶液的密度都为1g•cm-3];
⑤若用50mL 0.55mol•L-1的氨水(NH3•H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H会偏大(填“偏大”、“偏大”或“不变”,其原因是一水合氨为弱电解质,反应过程中电离需要吸收热量,故放出的热量偏少,△H偏大.
1.下列物质中,在一定条件下能水解的高分子化合物是( )
| A. | 肥皂 | B. | 油脂 | C. | 纤维素 | D. | 氨基酸 |
5.在铜的催化作用下氨气和氟气反应,得到两种氟化物,一种是离子化合物M,另一种是共价化合物N且其分子构型与氨气类似,下列有关说法错误的是( )
| A. | 该反应中氧化剂与还原剂物质的量之比为3:4 | |
| B. | 该反应中氧化产物与还原产物物质的量之比为1:4 | |
| C. | N是氧化产物,而且是极性分子 | |
| D. | M是还原产物,其还原性比NH3弱 |
3.设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 常温下1L0.1mol•L-1NH4NO3溶液中的氮原子数为0.2NA | |
| B. | 含1molH2SO4的浓硫酸和足量的锌完全反应,转移的电子数为2NA | |
| C. | A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,且D为强电解质(其他相关物质可能省略):A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C$\stackrel{H_{2}O}{→}$D,若A是共价化合物,0.1molA分子中含有的质子数可能为NA | |
| D. | 用足量CO还原磁铁矿得到9mol铁时转移24mol电子 |
2.H2、Cl2、O2组成混合气体,一定条件下恰好完全反应生成盐酸,则原混合气体中,H2、Cl2、O2的物质的量之比正确的是( )
| A. | 3:2:1 | B. | 6:1:2 | C. | 7:1:3 | D. | 7:4:1 |
20.设NA表示阿伏加德罗常数的,下列说法正确的是( )
| A. | 32 g氧气(O2)和32g臭氧(O3)所含氧原子数都为2NA | |
| B. | 18g水中所含电子数为8NA | |
| C. | 常温常压下,1 mol氖气原子数为2NA | |
| D. | 常温常压下,111.2L氮气所含氮原子数为NA |
19.下列有关物质检验方法不合理的是 ( )
0 157267 157275 157281 157285 157291 157293 157297 157303 157305 157311 157317 157321 157323 157327 157333 157335 157341 157345 157347 157351 157353 157357 157359 157361 157362 157363 157365 157366 157367 157369 157371 157375 157377 157381 157383 157387 157393 157395 157401 157405 157407 157411 157417 157423 157425 157431 157435 157437 157443 157447 157453 157461 203614
| A. | 向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显血红色,该溶液中一定含有Fe2+ | |
| B. | 用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2 | |
| C. | 检验Fe(NO3)2是否已氧化变质,可将Fe(NO3)2溶于稀H2SO4后滴加KSCN溶液,再观察溶液是否变血红 | |
| D. | 向某溶液中加NaOH溶液产生红褐色沉淀,说明溶液中含有Fe3+. |


