8. 一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
 一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )| A. | 反应的化学方程式为:2X?Y | B. | t1时,Y的浓度是X浓度的2倍 | ||
| C. | t2时,正反应速率大于逆反应速率 | D. | t3时,正逆反应速率相等,达到平衡 |
7.对于可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | NH3和H2O化学反应速率关系是2v正(NH3)=3v正(H2O) | |
| B. | 达到化学平衡时,4v正(O2)=5v逆(NO) | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 | |
| D. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
5.下列说法中正确的是( )
| A. | NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 | |
| B. | NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 | |
| C. | 在同一能级上运动的电子,其运动状态可能相同 | |
| D. | 若ABn的中心原子A上没有未用于形成共价键的孤对电子,当n=3,则分子结构为三角锥形 |
4.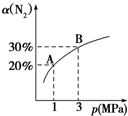 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )| A. | 平衡状态由A变到B时,平衡常数K(A)=K(B) | |
| B. | 将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ | |
| C. | 升高温度,逆反应速率增大,正反应速率减小 | |
| D. | 上述反应达到平衡后,增大H2浓度,平衡正向移动,H2转化率增大 |
3. 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为5Y?X | B. | t1时,Y的浓度是X浓度的2倍 | ||
| C. | t2时,正、逆反应速率相等 | D. | t3时,正、逆反应速率相等 |
2.与NH2-具有相同的质子数和电子数的微粒是( )
| A. | OH- | B. | NH4+ | C. | H3O+ | D. | CH4 |
20.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为化学计量数.在0~3min内,各物质物质的量的变化如表所示:
已知:2min内v(Q)=0.075mol•L-1•min-1,v(Z):v(Y)=1:2.
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度
(5)该反应达到化学平衡状态时D
A.反应停止了 B.正反应速率与逆反应速率均为0
C.反应物与生成物浓度相等 D.正反应速率与逆反应速率相等.
| 物质 | X | Y | Z | Q |
| 时间 | ||||
| 起始/mol | 0.7 | 1 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度
(5)该反应达到化学平衡状态时D
A.反应停止了 B.正反应速率与逆反应速率均为0
C.反应物与生成物浓度相等 D.正反应速率与逆反应速率相等.
19.表为元素周期表的一部分
回答下列问题
(1)Y元素在周期表中的位置为第二周期第ⅤIA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实不能说明Z 元素的非金属性比S 元素的非金属性强的是:b
a.Z的单质与H2S溶液反应,溶液变浑浊
b.Z的含氧酸HZO3酸性比H2SO4强
c.Z和S两元素的简单氢化物受热分解,前者的分解温度高
d.化合物SZ2中S显正价,Z显负价
(4)表中某元素的最高价含氧酸与其气态氢化物反应生成一种盐,该盐所含化学键的类型为离子键、共价键.
(5)碳、Y和硫三种元素按1:l:l个数比形成化合物,每个原子都达到8电子的稳定结构,该化合物的电子式为 .
.
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成两种有毒气体,均由表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和lmolO2,则两种气体的分子式及物质的量分别为NO 0.9mol,NO2 1.3mol,生成硫酸铜物质的量为2mol.
0 157265 157273 157279 157283 157289 157291 157295 157301 157303 157309 157315 157319 157321 157325 157331 157333 157339 157343 157345 157349 157351 157355 157357 157359 157360 157361 157363 157364 157365 157367 157369 157373 157375 157379 157381 157385 157391 157393 157399 157403 157405 157409 157415 157421 157423 157429 157433 157435 157441 157445 157451 157459 203614
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)Y元素在周期表中的位置为第二周期第ⅤIA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实不能说明Z 元素的非金属性比S 元素的非金属性强的是:b
a.Z的单质与H2S溶液反应,溶液变浑浊
b.Z的含氧酸HZO3酸性比H2SO4强
c.Z和S两元素的简单氢化物受热分解,前者的分解温度高
d.化合物SZ2中S显正价,Z显负价
(4)表中某元素的最高价含氧酸与其气态氢化物反应生成一种盐,该盐所含化学键的类型为离子键、共价键.
(5)碳、Y和硫三种元素按1:l:l个数比形成化合物,每个原子都达到8电子的稳定结构,该化合物的电子式为
 .
.(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成两种有毒气体,均由表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和lmolO2,则两种气体的分子式及物质的量分别为NO 0.9mol,NO2 1.3mol,生成硫酸铜物质的量为2mol.

 $\stackrel{HIO_{4}}{→}$
$\stackrel{HIO_{4}}{→}$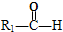 +
+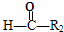 ,
,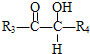 $\stackrel{HIO_{4}}{→}$
$\stackrel{HIO_{4}}{→}$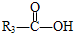 +
+
 .
. .
.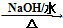 HOCH2CH2OH $\stackrel{HIO_{4}}{→}$HCHO
HOCH2CH2OH $\stackrel{HIO_{4}}{→}$HCHO 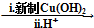 HCOOH
HCOOH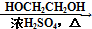 HCOOCH2CH2OOCH(合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物)
HCOOCH2CH2OOCH(合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物)