18.表为六种短周期元素的部分性质,下列有关说法错误的是( )
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.66 | 0.70 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A. | X与Y可以形成阴离子XY32- | |
| B. | Z的氢化物的沸点比T的氢化物的沸点高 | |
| C. | 元素R的氧化物对应水化物一定为强酸 | |
| D. | 由X形成的化合物QX和XR4,其晶体类型不相同 |
17.下列叙述中正确的是(NA为阿伏加德罗常数)( )
| A. | 1.7 g的羟基中含有的电子数为NA | |
| B. | 标准状况下,11.2 L四氯化碳所含的原子数为2NA | |
| C. | 常温常压下,18 g H2O含有的原子数为3NA | |
| D. | 5.6 g金属铁变为离子时失去的电子数为0.2NA |
16.已知:①C(s)+$\frac{1}{2}$O2(g)═CO(g);△H=-110.5kJ•mol-1
②C(s)+O2(g)═CO2(g);△H=-393.51kJ•mol-1
则反应C(s)+CO2(g)═2CO(g)的△H为( )
②C(s)+O2(g)═CO2(g);△H=-393.51kJ•mol-1
则反应C(s)+CO2(g)═2CO(g)的△H为( )
| A. | -283.01 kJ•mol-1 | B. | +172.51 kJ•mol-1 | ||
| C. | +283.01 kJ•mol-1 | D. | -172.51 kJ•mol-1 |
15.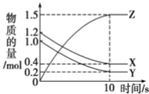 一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.则从反应开始到10s末的反应速率用X表示是( )
一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.则从反应开始到10s末的反应速率用X表示是( )
 一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.则从反应开始到10s末的反应速率用X表示是( )
一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.则从反应开始到10s末的反应速率用X表示是( )| A. | 0.08mol•L-1•s-1 | B. | 0.30mol•L-1•s-1 | C. | 0.16mol•L-1•s-1 | D. | 0.32mol•L-1•s-1 |
14.关于下列各实验装置的叙述中,正确的是( )


| A. | 装置①常用于分离互不相溶的液体 | B. | 装置②可用于吸收NH3 | ||
| C. | 装置③可用于收集NO、CO2等气体 | D. | 装置④可用于制备乙酸乙酯 |
12.下列实验相关叙述正确的是( )
| A. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| B. | 实验室常采用铁屑、溴水、苯混合制溴苯 | |
| C. | 苯中含有少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去 | |
| D. | 一定物质的量浓度溶液的配置必须要用干燥的容量瓶,否则有误差 |
10.下列物质中既含极性共价键又含有离子键的是( )
| A. | NaOH | B. | KCl | C. | HCl | D. | H2SO4 |
9.苯的结构式可用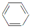 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )
0 157256 157264 157270 157274 157280 157282 157286 157292 157294 157300 157306 157310 157312 157316 157322 157324 157330 157334 157336 157340 157342 157346 157348 157350 157351 157352 157354 157355 157356 157358 157360 157364 157366 157370 157372 157376 157382 157384 157390 157394 157396 157400 157406 157412 157414 157420 157424 157426 157432 157436 157442 157450 203614
 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )| A. | 苯是无色无味,密度比水大的液体 | |
| B. | 苯中含有碳碳双键,所以苯属于烯烃 | |
| C. | 苯分子中6个碳碳化学键完全相同 | |
| D. | 苯可以与溴水、高锰酸钾溶液反应而使它们褪色 |
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:从反应开始到10s,X的物质的量减少了0.8 mol,Z的物质的量浓度增大了0.8 mol/L,用Z表示的反应速率为0.08 mol/(L•s).
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:从反应开始到10s,X的物质的量减少了0.8 mol,Z的物质的量浓度增大了0.8 mol/L,用Z表示的反应速率为0.08 mol/(L•s).