8.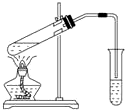 下列实验能获得成功的是( )
下列实验能获得成功的是( )
 下列实验能获得成功的是( )
下列实验能获得成功的是( )| A. | 用如图所示装置,无水乙酸和乙醇共热制取乙酸乙酯 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复原来的红色 | |
| C. | 水和乙醇的混合液,可用蒸馏的方法使其分离 | |
| D. | 淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可观察到有银镜出现 |
7.下列关于苯的叙述正确的是( )


| A. | 反应①为取代反应,有机产物的密度比水小 | |
| B. | 反应③为取代反应,有机产物是一种烃 | |
| C. | 反应④中1mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键 | |
| D. | 反应②为氧化反应,反应现象是火焰明亮并带有较多的黑烟 |
6.下列有关化学用语表示正确的是( )
| A. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | N2的电子式: | |
| C. | S2-的结构示意图: | |
| D. | 甲烷分子的比例模型是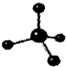 |
5.化学与生产和生活密切相关,下列说法正确的是( )
| A. | 利用化石燃料燃烧放出的热量使水分解制备氢气,是氢能开发的研究方向 | |
| B. | 石油的分馏和煤的干馏,都属于化学变化 | |
| C. | 向鸡蛋清的溶液中加入饱和(NH4)2SO4溶液,鸡蛋清因发生变性而析出 | |
| D. | 可利用二氧化碳制备全降解塑料 |
4.欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫.请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
5 C+4 KMnO4+6 H2SO4→5CO2↑+4MnSO4+2K2SO4+6H2O
(2)焦炭可用于制取水煤气.测得12g碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g)△H=+131.6kJ•mol-1.
(3)工业上在恒容密闭容器中用下列反应合成甲醇:
CO(g)+2H2(g)$?_{加热}^{催化剂}$CH3OH(g)△H=akJ/mol.
如表所列数据是反应在不同温度下的化学平衡常数(K).
①判断反应达到平衡状态的依据是BD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
②某温度下,将2mol CO和一定量的H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则以H2表示的反应速率v(H2)=0.16mol/(L•min).
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,其正极反应式:O2+2CO2+4e-═2CO32-,则负极反应式:2CO-4e-+2CO32-=4CO2.
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)═BaCO3(s)+SO42-(aq).已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=2.5×10-9.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
5 C+4 KMnO4+6 H2SO4→5CO2↑+4MnSO4+2K2SO4+6H2O
(2)焦炭可用于制取水煤气.测得12g碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g)△H=+131.6kJ•mol-1.
(3)工业上在恒容密闭容器中用下列反应合成甲醇:
CO(g)+2H2(g)$?_{加热}^{催化剂}$CH3OH(g)△H=akJ/mol.
如表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
②某温度下,将2mol CO和一定量的H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则以H2表示的反应速率v(H2)=0.16mol/(L•min).
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,其正极反应式:O2+2CO2+4e-═2CO32-,则负极反应式:2CO-4e-+2CO32-=4CO2.
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)═BaCO3(s)+SO42-(aq).已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=2.5×10-9.
3.下列关于各实验装置的叙述中,正确的是( )


| A. | ①装置可用于蒸干氯化铝溶液制AlCl3 | |
| B. | ②装置可用于分离CCl4萃取碘水后已分层的有机层和水层 | |
| C. | ③装置可用于收集NH3或HCl气体,并防止倒吸 | |
| D. | ④装置盐桥中的K+自右向左移动 |
2.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8g CH4含有4NA个氢原子 | |
| B. | 1 mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| C. | 1L 0.1 mol/L (NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 10 L pH=l 的硫酸溶液中含有的H+离子数为2NA |
1.以下有关主族元素原子的“未成对电子”的说法,正确的是( )
| A. | 核外电子数为奇数的基态原子,其原子轨道中一定不含有“未成对电子” | |
| B. | 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” | |
| C. | 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” | |
| D. | 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子” |
20.2011国际化学年主题是“化学-我们的生活,我们的未来”.下列叙述正确的是( )
0 157251 157259 157265 157269 157275 157277 157281 157287 157289 157295 157301 157305 157307 157311 157317 157319 157325 157329 157331 157335 157337 157341 157343 157345 157346 157347 157349 157350 157351 157353 157355 157359 157361 157365 157367 157371 157377 157379 157385 157389 157391 157395 157401 157407 157409 157415 157419 157421 157427 157431 157437 157445 203614
| A. | 利用太阳能、潮汐能、煤炭发电,以获取清洁能源 | |
| B. | 反应热等于恒压体系中,反应过程产生的焓变 | |
| C. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 | |
| D. | 纳米铜能在氧气中燃烧,说明了纳米铜比普通铜的还原性强 |