18.已知:H2CO3 Ka1=4.3×10-7Ka2=5.61×10-11
HClO Ka=2.95×10-8 CaCO3 Ksp=2.8×10-9
下列离子方程式书写正确的是( )
HClO Ka=2.95×10-8 CaCO3 Ksp=2.8×10-9
下列离子方程式书写正确的是( )
| A. | 向碳酸氢镁溶液中加入足量的氢氧化钡溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| B. | 向NaClO溶液通入少量CO2的离子反应方程式:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 用惰性电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 向Ca(ClO)2溶液中通入少量CO2的离子反应方程式:Ca2++2ClO-+CO2+H2O═2HClO+CaCO3↓ |
17.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 甲基橙呈黄色的溶液:Na+、Ba2+、AlO2-、Cl- | |
| B. | 由水电离得到的c(H+)=1×10-12的溶液中:K+、Na+、CH3COO-、Br- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、Cl-、NO3- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:$NH_4^+$、Al3+、$NO_3^-$、Cl- |
16.丙烯醇(CH2═CH-CH2OH)可发生的化学反应有( )
①加成②氧化③酯化④加聚⑤取代.
①加成②氧化③酯化④加聚⑤取代.
| A. | 只有①②③ | B. | 只有①②③④ | C. | ①②③④⑤ | D. | 只有①③④ |
14.苯与乙烯相比较,下列叙述不正确的是( )
| A. | 都能在空气中燃烧 | |
| B. | 都容易发生取代反应 | |
| C. | 苯和乙烯都能在一定条件下发生加成反应 | |
| D. | 苯不能使酸性KMnO4溶液褪色而乙烯能 |
13.电子计算器所用的纽扣式电池为银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Ag2O+Zn+H2O═Zn(OH)2+2Ag,下列叙述中正确的是( )
| A. | 电子由锌经导线流向Ag2O | |
| B. | 负极的电极反应为Zn-2e-═Zn2+ | |
| C. | 溶液中OH-向正极移动 | |
| D. | 随着电极反应的不断进行,电解质的碱性减弱 |
12.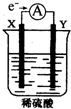 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | X极上发生的是还原反应 | |
| B. | 若两电极分别为Fe和碳棒,则Y为Fe | |
| C. | 若反应进行一段时间后,产生2克H2时转移了1mol电子 | |
| D. | 溶液中的SO42-向X极移动 |
11.下列各组顺序的排列正确的是( )
| A. | 单质氧化性:I2>Br2>Cl2 | B. | 热稳定性:PH3>H2S>HCl | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
10.下列化合物中,既含有离子键又含有共价键的是( )
| A. | CaO | B. | CaCl2 | C. | NaOH | D. | C2H6 |
9.下列有关化学用语使用正确的是( )
0 157248 157256 157262 157266 157272 157274 157278 157284 157286 157292 157298 157302 157304 157308 157314 157316 157322 157326 157328 157332 157334 157338 157340 157342 157343 157344 157346 157347 157348 157350 157352 157356 157358 157362 157364 157368 157374 157376 157382 157386 157388 157392 157398 157404 157406 157412 157416 157418 157424 157428 157434 157442 203614
| A. | F-的结构示意图: | |
| B. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | 氮气的电子式: | |
| D. | 乙烯的结构简式:CH2CH2 |
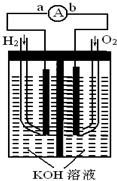 燃料电池是一种能量转换效率高、对环境友好的化学电源,图为一种氢氧燃料电池的结构装置.
燃料电池是一种能量转换效率高、对环境友好的化学电源,图为一种氢氧燃料电池的结构装置.