3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2L氟化氢中含有分子的数目为0.5NA | |
| B. | 常温下a克某烷烃(CnH2n+2)中含有共用电子对数目为$\frac{a}{14n+2}$(3n+1)NA | |
| C. | 56g 聚乙烯中含有碳碳双键的数目为2NA | |
| D. | 常温下,0.2mol/L的FeCl3溶液中含Cl-数目为0.6NA |
2.下列说法正确的是( )
| A. | 海洋约占地球表面积的71%,所以地球上不缺水 | |
| B. | 海水淡化蒸馏法的成本最低 | |
| C. | 海水淡化的主要方法有蒸馏法、电渗析法和离子交换法等 | |
| D. | 以上说法都正确 |
1.下列关于12C和13C说法正确的是( )
| A. | 两者互为同位素 | B. | 两者属于不同的元素 | ||
| C. | 两者属于同一种核素 | D. | 两者互为同素异形体 |
20.高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂.工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
则下列有关说法不正确的是( )
湿法制备的主要离子反应为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
则下列有关说法不正确的是( )
| A. | Na2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 | |
| B. | 湿法中FeO42-是氧化产物;干法中O2也是氧化产物 | |
| C. | 干法中每生成1mol Na2FeO4,这个反应共转移4mol电子 | |
| D. | 高铁酸钠中铁显+6价,它在氧化还原反应中通常被还原 |
19.下列有关化学用语表示正确的是( )
| A. | H2O2的电子式: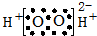 | B. | F-的结构示意图: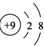 | ||
| C. | 中子数为20 的氯原子:2017Cl | D. | NH3的电子式: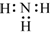 |
18.Na3N是离子化合物,它和水作用可产生NH3.下列叙述正确的是( )
| A. | Na3N与盐酸反应生成的都是盐 | |
| B. | Na+和N3-的电子层结构不相同 | |
| C. | Na+的半径大于N3-的半径 | |
| D. | 在Na3N与水的反应中,Na3N做还原剂 |
16.mmol C2H4跟 nmol H2在密闭容器中反应,生成pmol C2H6.将反应后的混合气体完全燃烧,生成CO2和H2O,所需氧气的物质的量是( )
| A. | 3.5 pmol | B. | (3m+$\frac{n}{2}$-3p)mol | C. | (3m+$\frac{n}{2}$)mol | D. | (3m+n)mol |
15.下列事实能用影响化学反应速率的外界条件来解释的是( )
0 157228 157236 157242 157246 157252 157254 157258 157264 157266 157272 157278 157282 157284 157288 157294 157296 157302 157306 157308 157312 157314 157318 157320 157322 157323 157324 157326 157327 157328 157330 157332 157336 157338 157342 157344 157348 157354 157356 157362 157366 157368 157372 157378 157384 157386 157392 157396 157398 157404 157408 157414 157422 203614
| A. | 镁和锌分别与相同浓度的盐酸反应,镁产生H2的速率快 | |
| B. | 铜与浓硝酸反应生成NO2,与稀硝酸反应生成NO | |
| C. | 用加热的方法可以将水中溶解的O-和N2赶出 | |
| D. | 面粉加工厂内充满粉尘,遇火易发生爆炸 |
 C:CH3COOH
C:CH3COOH .
.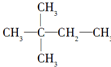 ,则A的结构简式为(CH3)3CCH=CH2.
,则A的结构简式为(CH3)3CCH=CH2.