11.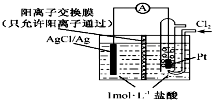 某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
 某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )| A. | 正极反应为AgCl+e-=Ag+Cl- | |
| B. | 电池工作时,交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 若用KCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.2 mol e-时,交换膜左侧溶液中约减少0.4 mol离子 |
10.短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数,且X、Y、W原子最外层电子数之和恰好等于Z元素的核电荷数,X与W的最高化合价之和为8,常见金属元素Z的一种核素的质量数为28,中子数比质子数多2.下列说法中正确的是( )
| A. | Y和W的含氧酸均为强酸 | |
| B. | YW3分子中Y原子的杂化方式为sp2,分子的空间构型为平面三角形 | |
| C. | 由非金属元素组成的化合物YX5是一种是否存在尚待确证的化合物,假如存在,该物质与水反应必然生成气体X2,同时得到一种弱碱溶液 | |
| D. | 因为Z的氧化物熔点很高,不适宜于电解,故工业上常用电解Z与W的化合物的方法制取单质Z |
9.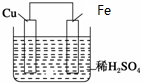 如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
①Fe为正极,Cu为负极; ②H+向负极移动;
③电子是由Fe经外电路流向Cu;④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为11.2L;
⑥负极的电极反应式为Fe-3e-═Fe3+.
0 157221 157229 157235 157239 157245 157247 157251 157257 157259 157265 157271 157275 157277 157281 157287 157289 157295 157299 157301 157305 157307 157311 157313 157315 157316 157317 157319 157320 157321 157323 157325 157329 157331 157335 157337 157341 157347 157349 157355 157359 157361 157365 157371 157377 157379 157385 157389 157391 157397 157401 157407 157415 203614
 如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )①Fe为正极,Cu为负极; ②H+向负极移动;
③电子是由Fe经外电路流向Cu;④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为11.2L;
⑥负极的电极反应式为Fe-3e-═Fe3+.
| A. | ①②③ | B. | ③④ | C. | ③④⑤ | D. | ③④⑥ |

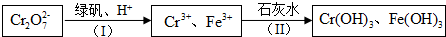
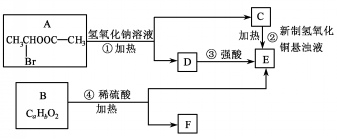
 .
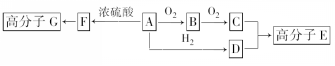
.
 .
. +2H2O.
+2H2O.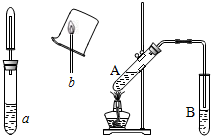 乙醇性质探究
乙醇性质探究