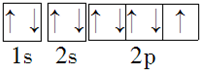
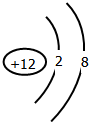
15.镁、锂在元素周期表中具有特殊“对角线”关系,它们的性质相似.例如,它们的单质在过量氧气中燃烧时均只生成正常的氧化物等,下列关于锂的叙述不正确的是( )
| A. | Li2SO4能溶于水 | |
| B. | LiOH是易溶于水、受热不分解的强碱 | |
| C. | Li遇浓硫酸不产生“钝化”现象 | |
| D. | Li2CO3受热分解,生成Li2O和CO2 |
14.与乙烯所含碳、氢元素的质量分数相同,但与乙烯既不是同系物又不是同分异构体的是( )
| A. | 环丙烷(C3H6) | B. | 乙烷 | C. | 甲烷 | D. | 丙烯(CH3CH═CH2) |
13.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 实验室从海带中提取单质碘的方法是取样→灼烧→溶解→过滤→萃取 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 为了增加食物的营养成分,可以大量使用食品添加剂 | |
| D. | 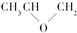 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则 ,该反应符合绿色化学的原则 |
10.分子式为C9H12的属于芳香烃的同分异构体(不考虑立体异构)共有( )
| A. | 2种 | B. | 5种 | C. | 8种 | D. | 11种 |
9.括号内物质为杂质,下列除去杂质的方法不正确的是( )
| A. | 乙酸乙酯(乙酸):用NaOH溶液洗涤后分液 | |
| B. | 乙烷(乙烯):用溴水洗气 | |
| C. | 溴苯(溴):用NaOH溶液洗涤后分液 | |
| D. | 乙醇(水):用生石灰吸水后蒸馏 |
8.A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如表:
(1)元素Y是C下一周期同主族元素,比较B、Y元素的第一电离能I1(B)>I1(Y)(填“>”“=”或“<”);
(2)盐X的水溶液呈酸性(填“酸性”“碱性”或“中性”),原因NH4++H2O?NH3•H2O+H+(用离子方程式表示);
(3)E元素原子的核外电子排布式为1s22s22p63s23p63d64s2,在周期表中的位置第四周期Ⅷ族;
(4)C单质分子中σ键和π键的个数比为1:2,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是NH3分子间存在氢键;
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式: ,写出该阳离子与硫的氢化物的水溶液反应的离子方程式:2H2O++H2S=S↓+2H2O+2H+.
,写出该阳离子与硫的氢化物的水溶液反应的离子方程式:2H2O++H2S=S↓+2H2O+2H+.
0 157204 157212 157218 157222 157228 157230 157234 157240 157242 157248 157254 157258 157260 157264 157270 157272 157278 157282 157284 157288 157290 157294 157296 157298 157299 157300 157302 157303 157304 157306 157308 157312 157314 157318 157320 157324 157330 157332 157338 157342 157344 157348 157354 157360 157362 157368 157372 157374 157380 157384 157390 157398 203614
| 元素 | 有关性质或结构信息 |
| A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
| B | B原子得到一个电子后3p轨道全充满 |
| C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
| D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物水化物的酸性为同主族最强 |
| E | E元素的核电荷数等于A原子的核电荷数和B元素氢化物的核电荷数之和 |
(2)盐X的水溶液呈酸性(填“酸性”“碱性”或“中性”),原因NH4++H2O?NH3•H2O+H+(用离子方程式表示);
(3)E元素原子的核外电子排布式为1s22s22p63s23p63d64s2,在周期表中的位置第四周期Ⅷ族;
(4)C单质分子中σ键和π键的个数比为1:2,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是NH3分子间存在氢键;
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式:
 ,写出该阳离子与硫的氢化物的水溶液反应的离子方程式:2H2O++H2S=S↓+2H2O+2H+.
,写出该阳离子与硫的氢化物的水溶液反应的离子方程式:2H2O++H2S=S↓+2H2O+2H+.