14.我国成功研制了铯(133Cs)原子喷泉钟.已知该铯原子的核外电子数为55,则该原子的中子数为( )
| A. | 23 | B. | 55 | C. | 78 | D. | 133 |
11.电池是人类生产和生活中的重要的能量来源,各式各样电池的发明是化学对人类的一项重大贡献.下列有关电池的叙述正确的是( )
| A. | 构成电池的两极必须是活泼性不同的金属 | |
| B. | 锌锰干电池工作时,锌作负极 | |
| C. | 在电池中,电子流出的一极是负极,发生还原反应 | |
| D. | 银锌纽扣电池工作时,电子由锌极流出经过溶液后流向银极 |
10.下列化学用语表述正确的是( )
| A. | 质子数为53、中子数为78的碘原子:13153I | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | CO2的球棍模型: | |
| D. | NH4I的电子式: |
9.常温下,将下列物质溶于水分别配成0.1mol.L-1溶液,所得溶液pH大于7的是( )
| A. | NaCl | B. | HCl | C. | CH3COONa | D. | NH4Cl |
8.下列关于钠的化合物叙述中错误的是( )
| A. | 1molNa2O2与2molNaHCO3固体混合物在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是NaOH和Na2CO3 | |
| B. | 由Na2O、Na2O2、Na2CO3•10H2O组成的混合物0.05 mol,溶于水后加入50 mL 2 mol/L的盐酸恰好完全反应,则原混合物中各成分的物质的量之比可以为任意值 | |
| C. | 向Na2 CO3饱和溶液中通入CO2,溶液变浑浊有晶体析出 | |
| D. | 将钠与氧气反应的生成物1.5 g溶于水,所得溶液恰好能被80 mL浓度为0.50 mol/L的HCl溶液中和,则该生成物的成分是Na2O和Na2O2 |
7.己知反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O;下列说法正确的是( )
0 157202 157210 157216 157220 157226 157228 157232 157238 157240 157246 157252 157256 157258 157262 157268 157270 157276 157280 157282 157286 157288 157292 157294 157296 157297 157298 157300 157301 157302 157304 157306 157310 157312 157316 157318 157322 157328 157330 157336 157340 157342 157346 157352 157358 157360 157366 157370 157372 157378 157382 157388 157396 203614
| A. | 1mol 氧化剂在反应中得到的电子为12mol | |
| B. | Cu(IO3)2既作氧化剂又作还原剂 | |
| C. | CuI中各元素化合价在反应前后都不变 | |
| D. | I2既作氧化产物又作还原产物 |
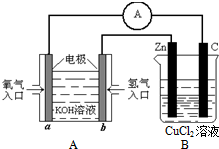 到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.