15.下列叙述不正确的是( )
| A. | 氢氧燃料电池是一种将化学能转化为电能的装置 | |
| B. | 铁船底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| C. | 钢铁腐蚀的负极反应:Fe-3e-═Fe3+ | |
| D. | 工业上电解饱和食盐水的阴极反应:2H++2e-═H2↑ |
14.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
| A. | 植物油不能使溴的四氯化碳溶液褪色 | |
| B. | 葡萄糖能发生水解反应 | |
| C. | 淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
13.下列物质加入水中,搅拌,最终浮于水上面的是( )
| A. | 溴乙烷 | B. | 溴苯 | ||
| C. | 乙醛 | D. | 高级脂肪酸甘油酯 |
11.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状态下,22.4L氯化氢中含有氯原子的数目为NA | |
| B. | 常温常压下,7.0g乙烯与丙稀的混合物中含有碳原子的数目为NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
10. 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
A通常显+3价,A的电负性>B的电负性(填“>”、“<”或“=”).
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据如表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3杂化.
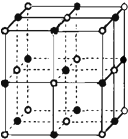
(3)实验证明:KCl、CaO这2种晶体的结构与NaCl晶体结构相似(如图所示):
则KCl、CaO这2种晶体熔点从高到低的顺序是:CaO>KCl,其原因是离子半径越小,离子所带电荷越多,晶格能越大,熔点越高 (从影响晶格能大小的因素进行描述).其中CaO晶体中一个Ca2+周围和它最邻近且等距离的Ca2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是CrO2.
 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据如表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3杂化.
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
则KCl、CaO这2种晶体熔点从高到低的顺序是:CaO>KCl,其原因是离子半径越小,离子所带电荷越多,晶格能越大,熔点越高 (从影响晶格能大小的因素进行描述).其中CaO晶体中一个Ca2+周围和它最邻近且等距离的Ca2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是CrO2.
9.下列关于电化学知识说法正确的是( )
| A. | 任何化学反应都可以设计成电解池反应 | |
| B. | 电解冶炼镁、铝通常电解MgCl2和Al2O3,也可电解MgO和 | |
| C. | 若把Cu+H2SO4═CuSO4+H2↑设计成电解池,应用Cu作阳极 | |
| D. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
8.下列说法中正确的是( )
①油脂在酸性或碱性条件下均可发生水解反应,且产物相同
②由油脂得到甘油和由淀粉得到葡萄糖均发生了水解反应
③淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
④用新制的银氨溶液可区分甲酸甲酯和乙醛.
①油脂在酸性或碱性条件下均可发生水解反应,且产物相同
②由油脂得到甘油和由淀粉得到葡萄糖均发生了水解反应
③淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
④用新制的银氨溶液可区分甲酸甲酯和乙醛.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
7.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 78 g Na2O2固体中含有的阴离子数为NA | |
| C. | 标准状况下,11.2 L CH3OH中含有的分子数目为0.5NA | |
| D. | 常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
6.提出元素周期律并绘制了第一个元素周期表的科学家是( )
0 157194 157202 157208 157212 157218 157220 157224 157230 157232 157238 157244 157248 157250 157254 157260 157262 157268 157272 157274 157278 157280 157284 157286 157288 157289 157290 157292 157293 157294 157296 157298 157302 157304 157308 157310 157314 157320 157322 157328 157332 157334 157338 157344 157350 157352 157358 157362 157364 157370 157374 157380 157388 203614
| A. | 盖斯 | B. | 阿伏加德罗 | C. | 门捷列夫 | D. | 道尔顿 |