10.已知:还原性强弱:I->Fe2+.往100mL碘化亚铁溶液中缓慢通入2.24L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+.则原碘化亚铁溶液的物质的量浓度为( )
| A. | 0.6 mol•L-1 | B. | 0.8 mol•L-1 | C. | 1.0 mol•L-1 | D. | 1.2 mol•L-1 |
9.海洋中有丰富的食品、矿产、能源、药物和水产资源.下图是从海水中提取某些原料的.
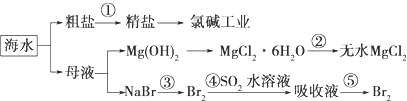
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液-→过滤后加盐酸 | |
| B. | 从第③步到第⑤步的目的是浓缩、富集溴 | |
| C. | 第①到第⑤步中,涉及到氧化还原反应共有2步 | |
| D. | 第④步中,SO2起氧化作用 |
7.工业上利用氢气在氯气中燃烧,所得产物再溶于水的方法制得盐酸,流程复杂且造成能量浪费.有人设想利用原电池原理直接制盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是( )
| A. | 通入氢气的电极为原电池的正极 | |
| B. | 两极材料都用石墨,用稀盐酸做电解质溶液 | |
| C. | 电解质溶液中的阳离子向通氯气的电极移动 | |
| D. | 通氯气的电极反应式为Cl2+2e-═2Cl- |
6.下列离子方程式正确的是( )
| A. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 在过氧化钠中加入稀硫酸:O22-+4H+═2H2O+O2↑ | |
| C. | 澄清石灰水与过量的小苏打溶液反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
5.已知放射性元素${\;}_{77}^{192}$Ir位于元素周期表中第六周期第Ⅷ族,下列关于${\;}_{77}^{192}$Ir的说法正确的是( )
0 157189 157197 157203 157207 157213 157215 157219 157225 157227 157233 157239 157243 157245 157249 157255 157257 157263 157267 157269 157273 157275 157279 157281 157283 157284 157285 157287 157288 157289 157291 157293 157297 157299 157303 157305 157309 157315 157317 157323 157327 157329 157333 157339 157345 157347 157353 157357 157359 157365 157369 157375 157383 203614
| A. | 铱为非金属元素 | |
| B. | ${\;}_{77}^{192}$Ir中子数与质子数的差为38 | |
| C. | 铱元素与碘元素位于同一周期 | |
| D. | ${\;}_{77}^{192}$Ir核外含有115个电子 |
 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二. 无色,无气味并且易燃.是常见的一种基础能源.
无色,无气味并且易燃.是常见的一种基础能源. 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.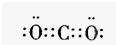 .
.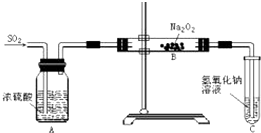 有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
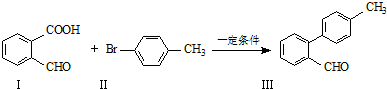
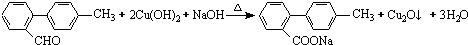 .
.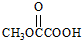 与
与  也可以发生类似反应①的反应,有机产物的结构简式为
也可以发生类似反应①的反应,有机产物的结构简式为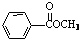 .
.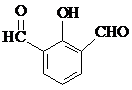 、
、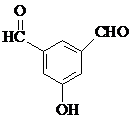 、
、 (要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)