13.下列物质中,属于有机物但不属于烃的是( )
| A. | CO | B. | CH3COOH | C. | CaCO3 | D. | C2H6 |
12.室温时,向一密闭容器中充入2mol SO2和2mol O2,在一定条件下发生反应:2SO2+O2?2SO3,该反应达到最大限度时,下列说法正确的是( )
| A. | 正反应的速率为零 | B. | SO2完全转化为SO3 | ||
| C. | SO3的物质的量浓度不再变化 | D. | SO2、O2和SO3的物质的量浓度相等 |
11.对于化学反应3W(g)+2X(g)═4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
| A. | υ(W)=3υ(Z) | B. | 3υ(X)=2υ(Z) | C. | υ(X)=2υ(Y) | D. | 3υ(W)=2υ(X) |
10.下列给出的有机物属于饱和烃的为( )
| A. | CCl4 | B. | C2H6 | C. | CH4 | D. | H2C═CH2 |
9.高温高压下,1L密闭容器中,发生如下反应:2H2+CO?CH3OH.反应开始时H2的物质的量为5mol,5min时变为0.5mol,则5min内该反应的平均反应速率v(H2)(单位:mol•L-1•min-1)为( )
| A. | 9.0 | B. | 0.9 | C. | 0.45 | D. | 4.5 |
7.某无色溶液中含有大量的H+和SO42-,则此溶液还能大量存在的离子组是( )
| A. | Na+、Fe2+、NO3- | B. | Na+、Mg2+、NO3- | ||
| C. | Cr2O72-、Ba2+、Cl- | D. | K+、Na+、S2O32- |
5.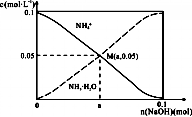 常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
0 157179 157187 157193 157197 157203 157205 157209 157215 157217 157223 157229 157233 157235 157239 157245 157247 157253 157257 157259 157263 157265 157269 157271 157273 157274 157275 157277 157278 157279 157281 157283 157287 157289 157293 157295 157299 157305 157307 157313 157317 157319 157323 157329 157335 157337 157343 157347 157349 157355 157359 157365 157373 203614
 常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )| A. | M点溶液中水的电离程度比原溶液小 | |
| B. | 据电荷守恒可知在M点时,n(OH-)-n(H+)=(a-0.05)mol | |
| C. | 当n(NaOH)=0.1mol时,c(Na+)=c(NH4+)+c(NH3•H2O) | |
| D. | 随着NaOH的加入,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$不断增大 |
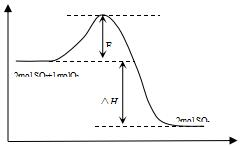 2SO2(g)+O2(g)?2SO3(g)△H<0,是工业制硫酸的主要反应之一.
2SO2(g)+O2(g)?2SO3(g)△H<0,是工业制硫酸的主要反应之一.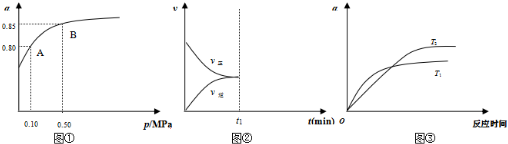
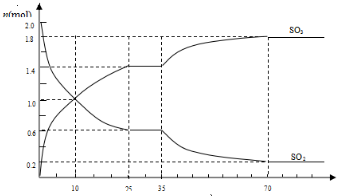
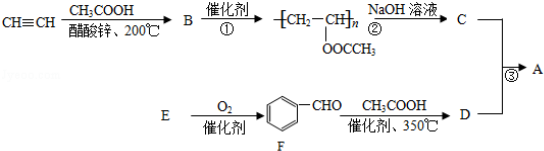

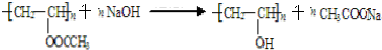 .
. .
. .
.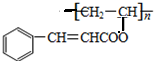 .
.