3.下列有关概念说法正确的是( )
| A. | ${\;}_{1}^{1}$H+、${\;}_{1}^{2}$H2、${\;}_{1}^{3}$H是氢元素的三种同位素 | |
| B. | CH2═CH2和  属于同系物 属于同系物 | |
| C. | 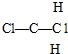 和 和 是甲烷的两种氯代物 是甲烷的两种氯代物 | |
| D. | 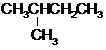 和 和 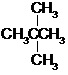 属于同分异构体 属于同分异构体 |
2.某烃的结构简式为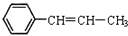 ,下列说法正确的是( )
,下列说法正确的是( )
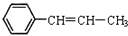 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 最多有16个原子共面 | |
| B. | 1mol该烃能与4molBr2发生加成反应 | |
| C. | 能发生聚合反应,其产物可表示为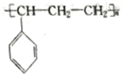 | |
| D. | 既能使溴的四氯化碳溶液褪色,又能使酸性高锰酸钾溶液褪色 |
1.化学科学需要借助化学语言来描述,下列化学用语正确的是( )
| A. | Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱 | |
| B. | NH4I的电子式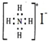 | |
| C. | 钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比不同 | |
| D. | Al2O3的化学键类型与AlCl3的化学键类型相同 |
20.某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是( )
| A. | 分子中的C、H、O的个数比为1:2:3 | |
| B. | 分子中C、H个数比为1:2 | |
| C. | 该有机物的相对分子质量为14的倍数 | |
| D. | 该分子中肯定不含氧元素 |
19.制烧碱所用盐水需两次精制.第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水.
已知:过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如表:
完成下列填空:
(1)过程Ⅰ除去的离子是SO42-.
(2)检测Fe3+是否除尽的方法是取少量过程II后的滤液于试管中,滴加几滴KSCN溶液,若溶液不变红,说明Fe3+已除尽,反之没除尽.
(3)过程Ⅰ选用BaCl2而不选用CaCl2,请运用表中数据解释原因BaSO4的溶解度比CaSO4的小,可将SO42-沉淀更完.
(4)除去Mg2+的离子方程式是2Mg2++2CO32-+H2O═Mg2(OH)2CO3↓+CO2↑.
(5)检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+即可,原因是在BaCO3、CaCO3、Mg2(OH)2CO3中,BaCO3的溶解度最大,若Ba2+沉淀完全,则说明Mg2+和Ca2+也沉淀完全.
第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:
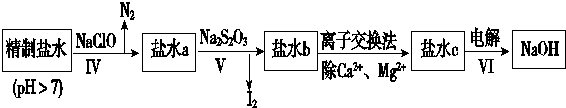
(6)过程Ⅳ除去的离子是NH4+、I-.
(7)过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释H+在阴极上得电子变成H2逸出,使H2O?H++OH-电离平衡向右移动,OH-在阴极区浓度增大,Na+向阴极区移动,最后NaOH在阴极区生成.
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水.
已知:过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如表:
完成下列填空:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
(2)检测Fe3+是否除尽的方法是取少量过程II后的滤液于试管中,滴加几滴KSCN溶液,若溶液不变红,说明Fe3+已除尽,反之没除尽.
(3)过程Ⅰ选用BaCl2而不选用CaCl2,请运用表中数据解释原因BaSO4的溶解度比CaSO4的小,可将SO42-沉淀更完.
(4)除去Mg2+的离子方程式是2Mg2++2CO32-+H2O═Mg2(OH)2CO3↓+CO2↑.
(5)检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+即可,原因是在BaCO3、CaCO3、Mg2(OH)2CO3中,BaCO3的溶解度最大,若Ba2+沉淀完全,则说明Mg2+和Ca2+也沉淀完全.
第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:

(6)过程Ⅳ除去的离子是NH4+、I-.
(7)过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释H+在阴极上得电子变成H2逸出,使H2O?H++OH-电离平衡向右移动,OH-在阴极区浓度增大,Na+向阴极区移动,最后NaOH在阴极区生成.
18.下列鉴别方法不可行的是( )
| A. | 用水鉴别乙醇、苯和溴苯 | |
| B. | 用饱和碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| C. | 用酸性高锰酸钾溶液鉴别乙烷、乙烯和二氧化硫气体 | |
| D. | 用溴水鉴别溴化钠、碘化钠和硫化钠 |
17.乙苯催化脱氢制苯乙烯反应: ,下列说法中不正确的是( )
,下列说法中不正确的是( )
 ,下列说法中不正确的是( )
,下列说法中不正确的是( )| A. | 乙苯的一氯代物共有 3 种不同结构 | |
| B. | 苯乙烯和氢气生成乙苯的反应属于加成反应 | |
| C. | 苯乙烯分子中所有原子有可能位于同一平面上 | |
| D. | 等质最的苯和苯乙烯燃烧耗氧量相同 |
16.有机物 的一氯代物可能的结构有(不考虑立体异构)( )
的一氯代物可能的结构有(不考虑立体异构)( )
0 157176 157184 157190 157194 157200 157202 157206 157212 157214 157220 157226 157230 157232 157236 157242 157244 157250 157254 157256 157260 157262 157266 157268 157270 157271 157272 157274 157275 157276 157278 157280 157284 157286 157290 157292 157296 157302 157304 157310 157314 157316 157320 157326 157332 157334 157340 157344 157346 157352 157356 157362 157370 203614
 的一氯代物可能的结构有(不考虑立体异构)( )
的一氯代物可能的结构有(不考虑立体异构)( )| A. | 3种 | B. | 5种 | C. | 6种 | D. | 8种 |
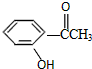 ②:
②: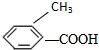
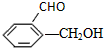 ④
④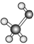 ⑤
⑤
 .
.