18.1mol下列有机物中与足量的NaHCO3溶液反应.可得2molCO2的是( )
| A. |  | B. | HOCH2CH2OH | C. | HOOC-COOH | D. | CH3COOH |
17.关于下列电解质溶液的说法中,正确的是( )
| A. | 常温下,10mL0.2mol/LNH4NO3溶液与10mL0.1mol/LNaOH溶液混合后所得pH=9.6的溶液中:c(NO3-)>c(NH4+)>c(Na+)>(NH3•H2O)>c(OH-)>c(H+) | |
| B. | 0.1mol•L-1Na2S溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) | |
| C. | 室温下,Ka(CH3COOH)=Kb(NH3•H2O)=1.7×10-5,则CH3COOH溶液中c(H+)和NH3•H2O溶液中的c(OH-)相等 | |
| D. | 室温下,向0.10mol•L-1的氨水中加入少量NaOH,溶液中c(NH${\;}_{4}^{+}$)减小,Kw减小 |
16.a L H2和CO的混合气体,充分燃烧后,消耗同温同压下氧气的体积是( )
| A. | a L | B. | $\frac{a}{2}$ L | C. | $\frac{a}{3}$ L | D. | 无法计算 |
15.在生活、工农业生产中都会用到物质分离的方法,下列分离方法与过滤原理相同的是( )
| A. | 含有泥沙的浑水,静置一会儿水沙分离,可取得上层的清水 | |
| B. | 农村“扬谷”分离饱满的谷粒和干瘪的谷壳 | |
| C. | 建筑工地上用铁筛把大小不同的沙粒分开 | |
| D. | 淘米除去米中混有的小沙粒 |
14.下面有关晶体的叙述中,错误的是( )
| A. | 白磷晶体中,分子之间通过共价键结合 | |
| B. | 金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | |
| C. | 在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-或(Na+) | |
| D. | 离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏 |
13.下列说法正确的是( )
| A. | NaCl晶体中每个钠离子与周围6个氯离子形成6个离子键 | |
| B. | 前四周期元素的原子中,未成对电子数最多的是Mn | |
| C. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| D. | 岩浆冷却过程中,晶格能高的矿物晶体先结晶 |
12.下列事实一定能说明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验灯泡很暗
③HNO2和NaCl不能发生反应
④0.1mol/LHNO2溶液的pH=2.1.
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验灯泡很暗
③HNO2和NaCl不能发生反应
④0.1mol/LHNO2溶液的pH=2.1.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
10.有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol•L-1,c(Cl-)为1.3mol•L-1.要使Mg2+全部转化为沉淀分离出来,至少需加4mol•L-1 NaOH溶液的体积为( )
| A. | 40 mL | B. | 72 mL | C. | 80 mL | D. | 128 mL |
9.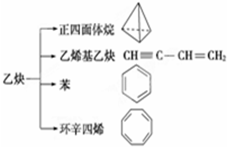 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
0 157143 157151 157157 157161 157167 157169 157173 157179 157181 157187 157193 157197 157199 157203 157209 157211 157217 157221 157223 157227 157229 157233 157235 157237 157238 157239 157241 157242 157243 157245 157247 157251 157253 157257 157259 157263 157269 157271 157277 157281 157283 157287 157293 157299 157301 157307 157311 157313 157319 157323 157329 157337 203614
 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )| A. | 正四面体烷的分子式为C4H4,其二氯代物有两种 | |
| B. | 苯为平面六边形结构,分子中存在C-C和C═C,能使酸性KMnO4溶液褪色 | |
| C. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 | |
| D. | 环辛四烯跟苯的结构很像,不能使溴水褪色 |