5.Al、Fe都是重要的金属元素.下列说法正确的是( )
| A. | 两者对应的氧化物均为碱性氧化物 | |
| B. | 两者的单质都不能与氢氧化钠溶液反应 | |
| C. | 常温条件下,两种金属都能溶解于浓硫酸中 | |
| D. | 制备AlCl3、FeCl3,均不能采用将其溶液直接蒸干的方法 |
4.下列说法正确的是( )
| A. | 摩尔是一种国际基本物理量 | |
| B. | 标准状况下气体摩尔体积约为22.4 L | |
| C. | 氢的摩尔质量是2 g/mol | |
| D. | 在同温同压下,相同体积的任何气体单质所含分子数相同 |
3.下列有关制备银镜过程说法正确的是( )
①边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水至最初的沉淀恰好溶解为止
②将几滴银氨溶液滴入2mL乙醛中
③银氨溶液具有较弱的氧化性
④在银氨溶液的配制过程中,溶液pH增大.
①边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水至最初的沉淀恰好溶解为止
②将几滴银氨溶液滴入2mL乙醛中
③银氨溶液具有较弱的氧化性
④在银氨溶液的配制过程中,溶液pH增大.
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
20.几种短周期元素的原子半径和主要化合价见表,下列有关说法中,正确的是( )
| 元素符号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
| A. | 离子半径大小:r(X2+)>r(Q2-) | |
| B. | Y与Q形成的化合物不能跟氢氧化钠溶液反应 | |
| C. | M元素与L元素形成的一种化合物是常见的有机溶剂 | |
| D. | Z的单质可在氧气中燃烧生成ZO3 |
18.类推是中学化学中重要的思维方法.下列类推结论正确的是( )
0 157084 157092 157098 157102 157108 157110 157114 157120 157122 157128 157134 157138 157140 157144 157150 157152 157158 157162 157164 157168 157170 157174 157176 157178 157179 157180 157182 157183 157184 157186 157188 157192 157194 157198 157200 157204 157210 157212 157218 157222 157224 157228 157234 157240 157242 157248 157252 157254 157260 157264 157270 157278 203614
| A. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 铝和硫加热得到Al2S3,故铁和硫加热得到Fe2S3 | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
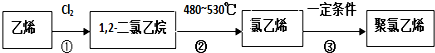
 ,反应类型为加聚反应;
,反应类型为加聚反应;
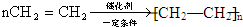 .
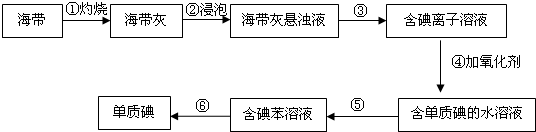
.
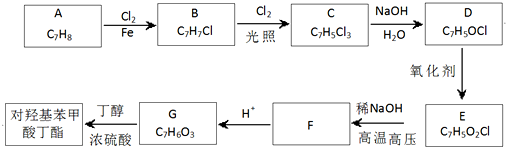
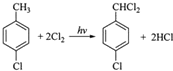 ;
; ;
; ;
;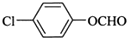 (写结构简式).
(写结构简式).