5.根据原子结构及元素周期律的知识,下列叙述正确的是( )
| A. | 由于分子中氢原子数:H2SO4>HClO4,故酸性:H2SO4>HClO4 | |
| B. | 硅处于金属与非金属的过渡位置,硅可用作半导体材料 | |
| C. | 由于氮元素的最低化合价只有-3价,故NH5这种物质不可能存在 | |
| D. | Cl-、S2-、Ca2+、K+半径逐渐减小 |
4.下列反应类型说法不正确的是( )
| A. | 2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2 氧化还原反应 | |
| B. | N2+3H2$?_{高温高压}^{催化剂}$2NH3可逆反应 | |
| C. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl 置换反应 | |
| D. | CH2=CH2+Br2→CH2Br-CH2Br 加成反应 |
2.下列叙述中,错误的是( )
| A. | 只含非极性键的纯净物一定是单质 | B. | 只含极性键的纯净物一定是化合物 | ||
| C. | 离子化合物中一定有离子键 | D. | 纯净物中一定存在化学键 |
1.下列装置或操作能达到实验目的是( )
| A. |  量取8.5mL稀硫酸 | B. | 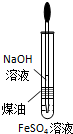 制备Fe(OH)2 | ||
| C. | 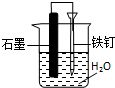 防止铁钉生锈 | D. | 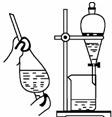 用酒精萃取水中的溴 |
20.某无色溶液中含有大量的H+和SO42-,则此溶液还能大量存在的离子组是( )
| A. | Na+、Fe2+、NO3- | B. | Na+、Mg2+、NO3- | C. | Cu2+、Ba2+、Cl- | D. | K+、Na+、HCO3- |
19.科学家预测原子序数为114的元素,它的位置在第7周期IVA族,称为类铅.关于它的性质,预测错误的是( )
| A. | 它的最外层电子数为4 | B. | 它的金属性比铅强 | ||
| C. | 它具有+2、+4价 | D. | 它的最高价氧化物的水化物是强酸 |
17.氨气分子的立体构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A. | 两种分子的中心原子的杂化轨道类型不同,NH3为sp2杂化,而CH4是sp3杂化 | |
| B. | NH3分子中氮原子形成3个杂化轨道,CH4分子中碳原子形成4个杂化轨道 | |
| C. | NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 | |
| D. | 氨气分子是四原子化合物,甲烷为五原子化合物 |
16.下列实验装置图正确的是( )
0 157016 157024 157030 157034 157040 157042 157046 157052 157054 157060 157066 157070 157072 157076 157082 157084 157090 157094 157096 157100 157102 157106 157108 157110 157111 157112 157114 157115 157116 157118 157120 157124 157126 157130 157132 157136 157142 157144 157150 157154 157156 157160 157166 157172 157174 157180 157184 157186 157192 157196 157202 157210 203614
| A. | 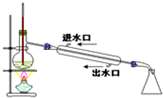 工业乙醇的蒸馏 | B. | 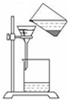 苯甲酸趁热过滤 | ||
| C. | 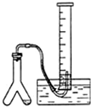 制少量乙炔并测体积 | D. | 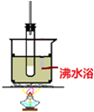 实验室制硝基苯 |
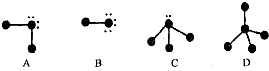
 ,含有的化学键离子键、极性键.
,含有的化学键离子键、极性键.