18.在某无色溶液中,可能存在Na+、Ca2+、Fe3+、Br-、CO32-、SO42-、Cl-中的几种.某同学进行了下列实验:
①取少量原溶液,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色,将溶液分为2份;
②一份中加入AgNO3溶液,有白色沉淀产生;
③另一份加入BaCl2溶液,有白色沉淀产生.
则该溶液中一定大量存在的离子组是( )
①取少量原溶液,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色,将溶液分为2份;
②一份中加入AgNO3溶液,有白色沉淀产生;
③另一份加入BaCl2溶液,有白色沉淀产生.
则该溶液中一定大量存在的离子组是( )
| A. | Na+、Fe3+、SO42- | B. | CO32-、Cl-、SO42- | C. | Ca2+、Br-、SO42- | D. | Na+、SO42-、CO32- |
17.现有含W g碳酸钙和a g二氧化硅的混合物,在高温下反应最终可生成标准状况下的气体体积为( )
| A. | $\frac{a}{60}×22.4$L | B. | $\frac{W}{100}×22.4$L | C. | $\frac{W-a}{40}×22.4$L | D. | 无法计算 |
16.Al与Na2O2的混合物溶于足量的水中,得到澄清溶液,同时产生3.5g气体.在所得溶液与100mL 7mol/L盐酸作用过程中,先有白色沉淀生成,此后沉淀又恰好溶解,则Al与Na2O2的物质的量之比为( )
| A. | 2:1 | B. | 1:2 | C. | 11:2 | D. | 2:11 |
15.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、电子天平、药匙、量筒、玻璃棒、500 mL容量瓶、胶头滴管.(在横线上填写所缺仪器的名称)
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
13.为了检验FeSO4溶液是否变质,最佳实验方法是取少量该溶液,向其中加入( )
| A. | NaOH溶液 | B. | 铁片 | C. | KSCN溶液 | D. | 石蕊溶液 |
12.有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D导线C;③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.据此,判断四种金属的活动性顺序是( )
| A. | A>B>C>D | B. | A>C>D>B | C. | C>A>D>B | D. | C>B>D>A |
11.如表为元素周期表的一部分,其中A、X、Y、W、Z为短周期元素,W元素的核电荷数为X元素的2倍.据此,下列说法中错误的是( )
| X | |||
| Y | Z | W | A |
| T | B |
| A. | X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反 | |
| B. | Y、Z、W、A元素性质均较为活泼,但其中Y、W在自然界中存在游离态的形式,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阳离子交换膜,其阴极反应式为:2H2O+2e-═2OH-+H2↑ | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2W3具有氧化性和还原性 |
10.2molFeCl2与1molCl2恰好完全反应,则转移的电子的物质的量为( )
0 157010 157018 157024 157028 157034 157036 157040 157046 157048 157054 157060 157064 157066 157070 157076 157078 157084 157088 157090 157094 157096 157100 157102 157104 157105 157106 157108 157109 157110 157112 157114 157118 157120 157124 157126 157130 157136 157138 157144 157148 157150 157154 157160 157166 157168 157174 157178 157180 157186 157190 157196 157204 203614
| A. | 4mol | B. | 3mol | C. | 2mol | D. | 1mol |
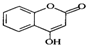 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: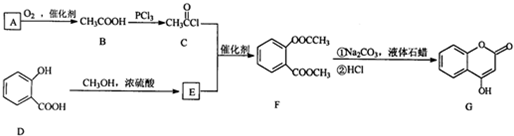
 .
.