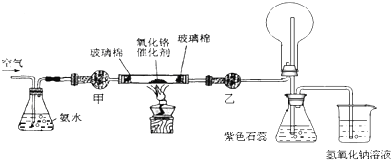
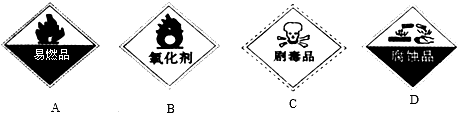
9.向分别盛有100mL水、100mL 0.1mol•L-1盐酸、100mL 0.01mol•L-1硫酸铜溶液的X、Y、Z三个烧杯中各投入0.05mol Na.下列有关说法正确的是( )
| A. | 三个烧杯中均会发生的离子反应为2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 三个烧杯中钠均在液面上剧烈反应,且X烧杯中反应最剧烈 | |
| C. | 三个烧杯反应后,生成的溶质的物质的量浓度相同 | |
| D. | 三个烧杯反应后,生成的气体的质量一定相同 |
7.用NA表示阿伏加德罗常数之值,下列说法正确的是( )
| A. | 2.3g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA | |
| B. | 1molNa2CO3晶体中含CO32-离子数小于NA | |
| C. | 惰性电极电解食盐水,若线路中通过NA电子电量,则阳极产生气体11.2L | |
| D. | 0.1molCaO2(过氧化钙)中含阴离子数是0.2NA |
6.相同温度下,将等体、积等pH的醋酸和盐酸溶液,分别加入V1 mL、V2mL的水稀释后,测得溶液的pH仍然相同,则下列关系正确的是( )
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | 无法判断 |
5.汽车的启动电源常用铅蓄电池,该电池在放电时的反应为PbO2(s)+Pb(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l),根据此反应判断下列叙述中正确的是( )
| A. | PbO2是电池的负极 | |
| B. | 负极的电极反应式为:Pb+SO42--2e-═PbSO4 | |
| C. | 铅蓄电池放电时,每转移2mol电子时消耗1mol硫酸 | |
| D. | 电池放电时,两极质量均增加,且每转移1mol电子时正极质量增加48g |
4.被称为“软电池”的纸质电池,采用有关薄层纸片作为一边镀锌,而在其另一边镀二氧化锰.在纸内的离子“流过”水和氧化锌组成的电解液.总反应的化学方程式为Zn+2MnO2+H2O═Zn(OH)2+Mn2O2,下列说法不正确的是( )
| A. | 该电池为一次电池 | |
| B. | 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═Mn2O3+2OH- |
3.如图是部分短周期元素原子半径与原子序数的关系图,下列说法错误的是( )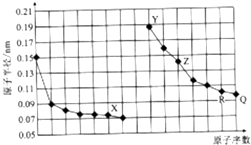

| A. | QX2、RX2都有杀菌消毒的作用,二者常用于自来水消毒 | |
| B. | 简单离子的半径:X>Y>Z | |
| C. | Y、Z、R对应的最高氧化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
1.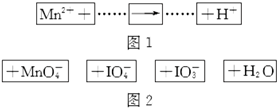 把图2的碎纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平).下列对该反应的说法不正确的是( )
把图2的碎纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平).下列对该反应的说法不正确的是( )
 把图2的碎纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平).下列对该反应的说法不正确的是( )
把图2的碎纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平).下列对该反应的说法不正确的是( )| A. | IO4-作氧化剂 | |
| B. | 若有1mol Mn2+参加反应转移5 mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 配平后Mn2+、H+的化学计量数分别为2、3 |
20.向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色.再向反应后的混合物中不断通人 SO2气体,溶液逐渐变成无色.下列分析不正确的是( )
0 156999 157007 157013 157017 157023 157025 157029 157035 157037 157043 157049 157053 157055 157059 157065 157067 157073 157077 157079 157083 157085 157089 157091 157093 157094 157095 157097 157098 157099 157101 157103 157107 157109 157113 157115 157119 157125 157127 157133 157137 157139 157143 157149 157155 157157 157163 157167 157169 157175 157179 157185 157193 203614
| A. | 滴加KI溶液时,转移2 mol e-时生成 1 mol白色沉淀 | |
| B. | 通入SO2后溶液逐渐变成无色,不是 SO2的漂白性 | |
| C. | 通入SO2时,SO2与I2反应,I2作氧化剂 | |
| D. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |