1.下列说法不正确的是( )
| A. | CH3COONa与CH3COOH混合溶液呈中性,则溶液中有c(CH3COO-)═c (Na+) | |
| B. | NaHCO3溶液中有:c (H+)+c (H2CO3)═c (OH-)+c (CO32-) | |
| C. | 物质的量浓度均为0.1 mol/L的Na2CO3和NaHCO3的混合溶液中有:c (Na+)>c (HCO3-)>c (CO32-)>c (OH-)>c (H+) | |
| D. | 常温下,p H为2的某酸HA与pH为12的某碱BOH等体积混合溶液呈酸性,则HA为强酸BOH为弱碱 |
20.用NA表示阿伏加德罗常数值,下列说法正确的是( )
| A. | 25℃时,pH=12的1.0L的NaClO溶液中水电离出的OH-的数目为0.01NA | |
| B. | 标准状况下,22.4L甲醇中含有的氧原子数为1.0NA | |
| C. | 标准状况下,22.4L氯气与足量NaOH溶液反应转移的电子数为2NA | |
| D. | 同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
19.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化.在变化的各阶段被破坏的粒子间的主要相互作用依次是( )
| A. | 氢键 分子间作用力 非极性键 | |
| B. | 氢键 极性键 分子间作用力 | |
| C. | 氢键 氢键 极性键 | |
| D. | 分子间作用力 氢键 非极性键 |
18.如表实验操作、现象和结论均正确的是选项实验操作现象结论( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 向稀硝酸溶液中加入过量铁粉充分反应后,滴加KSCN溶液 | 溶液变为血红色 | 稀硝酸具有氧化性,能将Fe氧化成Fe3+ |
| C | KNO3和KOH混合溶液中加入铝粉 并加热,管口放湿润的红色石蕊试纸 | 试纸变为蓝色 | NO3-还原为NH3 |
| D | 向两份蛋白质溶液中分别滴加 Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| A. | A | B. | B | C. | C | D. | D |
17.现有7种元素的性质、数据如表所列,它们属于第二或第三周期.
回答下列问题:
(1)③原子结构示意图是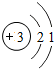 ,⑤的氢化物和⑦的氢化物形成化合物的电子式
,⑤的氢化物和⑦的氢化物形成化合物的电子式 .
.
(2)在最高价氧化物的水化物中,碱性最强的化合物的电子式是: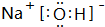 ; 属离子化合物(填“离子”或“共价”).
; 属离子化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用化学式表示):NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
编号 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| -2 | -3 | -1 | -3 |
(1)③原子结构示意图是
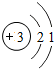 ,⑤的氢化物和⑦的氢化物形成化合物的电子式
,⑤的氢化物和⑦的氢化物形成化合物的电子式 .
.(2)在最高价氧化物的水化物中,碱性最强的化合物的电子式是:
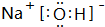 ; 属离子化合物(填“离子”或“共价”).
; 属离子化合物(填“离子”或“共价”).(3)比较④和⑦的氢化物的稳定性(用化学式表示):NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
16.化合物是一种取代有机氯农药DDT的新型杀虫剂,它含有几种官能团( )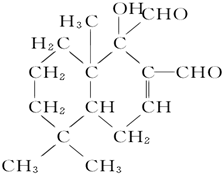

| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
15.下列措施一定能使化学反应速率降低的是( )
| A. | 增大反应物的浓度 | B. | 使用催化剂 | ||
| C. | 降低温度 | D. | 将块状固体变成粉末 |
14.一定量的盐酸与过量的铁粉反应时,为了减缓反应速率且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体;②Na2SO4溶液;③KNO3溶液;④H2O;⑤CaCO3固体;⑥NaCl固体.
①NaOH固体;②Na2SO4溶液;③KNO3溶液;④H2O;⑤CaCO3固体;⑥NaCl固体.
| A. | ①②⑤ | B. | ②③⑥ | C. | ②③④⑤ | D. | ②④ |
13.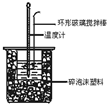 中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
0 156979 156987 156993 156997 157003 157005 157009 157015 157017 157023 157029 157033 157035 157039 157045 157047 157053 157057 157059 157063 157065 157069 157071 157073 157074 157075 157077 157078 157079 157081 157083 157087 157089 157093 157095 157099 157105 157107 157113 157117 157119 157123 157129 157135 157137 157143 157147 157149 157155 157159 157165 157173 203614
 中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )| A. | 改用60mL 0.50mol/L盐酸跟50mL 0.55 mol/L NaOH溶液进行反应,求出的中和热数值和原来相同 | |
| B. | 用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验比用 50mL0.50mol/L盐酸和50mL0.50mol/LNaOH测得的数值准确 | |
| C. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌 | |
| D. | 装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失 |
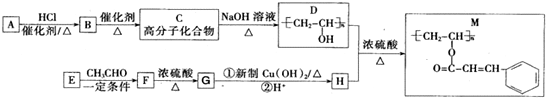

 .
.
 .
.